2013-2014 Rapports sur les plans et les priorités
Conseil d'examen du prix des médicaments brevetés
L'honorable Leona Aglukkaq
Ministre de la Santé
Table des matières
Message de la présidente
Section I : Survol de l'organisation
Section II : Analyse des programmes par résultat stratégique.
Section III : Renseignements supplémentaires
Section IV : Autres sujets d'intérêt
Notes en fin d'ouvrage
Message de la présidente
J'ai le plaisir de vous présenter le Rapport sur les plans et les priorités de 2013-2014 du Conseil d'examen du prix des médicaments brevetés (CEPMB).
Nous avons célébré en décembre 2012 le 25e anniversaire de l'organisme. Le CEPMB a été créé en 1987 en vertu de modifications apportées à la Loi sur les brevets, dans le but de protéger les consommateurs en veillant à ce que les prix des médicaments brevetés ne soient pas excessifs. Vingt-cinq ans plus tard, le CEPMB continue de contribuer au système de soins de santé canadien en jouant le même rôle essentiel quant à la protection des consommateurs et en faisant rapport des tendances relatives aux produits pharmaceutiques.
L'année dernière, le CEPMB a amorcé une évaluation de programme dans le but d'évaluer la mesure dans laquelle il atteint ses résultats, et que les ressources sont adaptées à l'exécution efficace de son mandat. L'évaluation prévoyait l'optimisation des ressources en y incluant des conclusions claires et valides sur la pertinence et le rendement des programmes du CEPMB. On a jugé que le Programme de réglementation du prix des médicaments brevetés et le Programme sur les tendances relatives aux produits pharmaceutiques (Programme de réglementation et Programme sur les tendances) pouvaient être appliqués par un organisme fédéral et cadraient bien avec les priorités pangouvernementales de même qu'avec le résultat stratégique du CEPMB. L'examen a permis de constater que le CEPMB parvient à atteindre ses résultats escomptés. Selon l'évaluation, le financement par reconduction qui a été reçu en 2008-2009 a été utilisé de façon efficace et a permis d'obtenir les résultats pour lesquels il avait été autorisé. Le Conseil prépare à l'heure actuelle une réponse et un plan d'action de la direction pour aborder les considérations soulevées dans le rapport d'évaluation. Ces documents sont affichés sur le site Web du CEPMB sous la rubrique « Responsabilisation ».
Pour l'année à venir, les priorités du CEPMB sont de poursuivre la mise en œuvre du plan d'action de la direction donnant suite au Rapport d'évaluation des programmes en cherchant des façons d'accélérer les processus du CEPMB, de simplifier davantage les Lignes directrices, d'alléger le fardeau réglementaire et d'utiliser efficacement les ressources du personnel du Conseil. Ce dernier objectif sera réalisé par l'intermédiaire d'un examen des exigences réglementaires du CEPMB et de sa planification de la relève.
Le Plan de surveillance et d'évaluation des principales modifications aux Lignes directrices du CEPMB a été en mesure d'ouvrir un dialogue continu avec les brevetés et les intervenants, ce qui nous permet d'être plus réceptifs et d'apporter des modifications à nos Lignes directrices en temps opportun. Le Conseil entend modifier les Lignes directrices de sorte qu'elles tiennent compte des changements dans l'environnement de la distribution et de l'établissement des prix des médicaments, et ce, selon un échéancier approprié. À mesure qu'il évolue, le CEPMB continuera d'accroître l'efficacité de ses programmes en suivant les conséquences de ses Lignes directrices, en les précisant et en les modifiant au besoin. Il restera en outre à l'affût d'occasions de mettre, en temps opportun, ses études et ses rapports à la disposition des décideurs en matière de politique.
En tant que présidente du CEPMB, mon but est de s'assurer que notre cadre continue d'influer de façon positive sur les consommateurs tout en tenant compte de la valeur qu'offrent les médicaments novateurs aux patients. Le CEPMB est toujours aussi déterminé à relever les défis avec efficacité, à servir les Canadiens et à contribuer au fonctionnement du système de soins de santé.
Mary Catherine Lindberg
Section I : Survol de l'organisation
Raison d'être
Créé par le Parlement en 1987, le Conseil d'examen du prix des médicaments brevetés (CEPMB) est un organisme indépendant qui détient des pouvoirs quasi judiciaires. Il est investi d'un double mandat :
- Réglementation — Veiller à ce que les prix auxquels les brevetés vendent leurs médicaments brevetés au Canada ne soient pas excessifs.
- Rapport — Faire rapport des tendances des prix de tous les médicaments ainsi que des dépenses des brevetés dans la R-D au Canada.
Dans l'exécution de son mandat, le CEPMB veille à la protection des Canadiens en s'assurant que les médicaments brevetés ne sont pas vendus au Canada à des prix excessifs et que les intervenants sont tenus informés des tendances relatives aux produits pharmaceutiques.
Responsabilités
Le CEPMB a été créé en 1987 en vertu de la Loi sur les brevets (la Loi) dans sa version modifiée (projet de loi C-22). La Loi a été modifiée à nouveau en 1993 (projet de loi C-91). Les révisions visaient à établir un juste équilibre entre la prolongation de la période de protection associée au brevet et la nécessité de protéger les intérêts des consommateurs en s'assurant que les médicaments brevetés ne sont pas vendus au Canada à des prix excessifs.
En raison de son double mandat, le CEPMB doit s'acquitter de deux responsabilités :
Réglementation du prix des médicaments brevetés
Il incombe au CEPMB de s'assurer que les prix départ-usine, à savoir les prix auxquels les brevetés vendent, au Canada, à leurs différents clients (grossistes, hôpitaux, pharmacies et autres) leurs médicaments brevetés pour usage humain ou pour usage vétérinaire distribués sous ordonnance ou en vente libre, ne sont pas excessifs. Le CEPMB réglemente le prix de chaque médicament breveté auquel Santé Canada a attribué un numéro d'identification du médicament (DIN) dans le cadre de son processus d'examen. Le mandat du Conseil couvre également les médicaments distribués au titre du Programme d'accès spécial ou distribués en vertu du programme d'essais cliniques de même que les drogues nouvelles de recherche. Les médicaments brevetés en vente libre et les médicaments brevetés à usage vétérinaire sont également réglementés par le Conseil en fonction des plaintes reçues.
Dans le cas où, à l'issue d'une audience publique, le Conseil juge que le prix d'un médicament breveté vendu sur un marché canadien est ou était excessif, il peut rendre une ordonnance obligeant le breveté à réduire le prix de son médicament et à appliquer les mesures qui lui sont dictées pour rembourser les recettes excessives qu'il a tirées de la vente de son médicament à un prix excessif.
Rapport sur les tendances relatives aux produits pharmaceutiques
Chaque année, le CEPMB rend compte au Parlement, par le truchement du ministre de la Santé, de ses principales activités, de ses analyses du prix des médicaments brevetés et des tendances relatives aux produits pharmaceutiques ainsi que des dépenses de R-D déclarées par les sociétés pharmaceutiques détentrices de brevets. Outre son rapport annuel, le CEPMB rend compte de ses activités dans son bulletin trimestriel La Nouvelle et dans diverses études.
En vertu de l'initiative du Système national d'information sur l'utilisation des médicaments prescrits (SNIUMP)i, le CEPMB effectue des analyses critiques des tendances relatives aux prix, à l'utilisation et aux coûts des médicaments au Canada. Ces analyses viennent appuyer le processus décisionnel en matière de politique des régimes d'assurance-médicaments fédéraux, provinciaux et territoriaux participants.
Résultat stratégique et Architecture d'harmonisation des programmes (AHP)
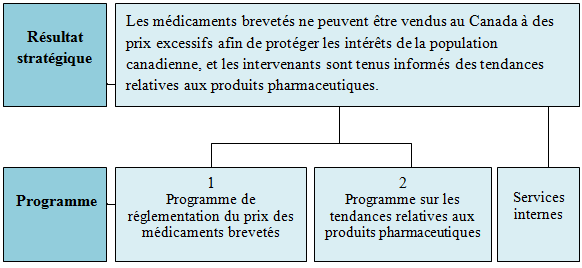
Résultat stratégique et Architecture d'harmonisation des programmes (AHP)
Le tableau qui suit illustre le résultat stratégique et les trois programmes du Conseil d'examen du prix des médicaments brevetés.
Priorités organisationnelles
| Priorité |
Type1 |
Résultat stratégique et (ou) programmes2 |
|
1 Les différents types de priorités sont définis comme suit : priorité déjà établie – établie au cours du premier ou du deuxième exercice précédant l'exercice visé par le rapport; priorité permanente – établie au moins trois exercices avant l'exercice visé par le rapport; priorité nouvelle – établie au cours de l'exercice visé par le RPP ou le RMR.
2 Le CEPMB n'a qu'un résultat stratégique. Ainsi, toutes les priorités se rapportent à ce résultat. Vous trouverez dans la présente colonne les liens menant aux programmes, pour chaque priorité.
|
| Poursuivre la mise en œuvre du plan d'action de la direction donnant suite au Rapport d'évaluation des programmes du CEPMB |
Déjà établie |
Liens aux programmes 1 et 2 |
| Description |
|
Pourquoi s'agit-il d'une priorité?
Bien que l'évaluation de 2011-2012 ait confirmé la pertinence, le rendement, l'efficacité et la rentabilité du Programme de réglementation du prix des médicaments brevetés et du Programme sur les tendances relatives aux produits pharmaceutiques, on a cerné quatre éléments à prendre en compte à l'égard du Conseil :
- Accélérer les processus du CEPMB – des processus plus rapides se traduiraient par des résultats plus rapides; cela pourrait notamment permettre une utilisation plus efficace des ressources, l'abrégement des périodes où les prix sont excessifs, un accès plus rapide aux renseignements sur les tendances relatives aux prix, aux ventes et à l'utilisation qui pourraient mener à un usage accru des renseignements produits par le CEPMB.
- Simplifier davantage les Lignes directrices – les intervenants sont préoccupés par le degré de complexité inhérent aux Lignes directrices qui, selon eux, nuit à la prévisibilité du processus de réglementation. Le fait de simplifier davantage les Lignes directrices pourrait les rendre plus prévisibles et moins susceptibles de différentes interprétations, ce qui pourrait accroître l'observation des Lignes directrices.
- Encourager l'utilisation d'un langage clair dans toutes les publications du CEPMB – certains intervenants ont souligné le besoin d'avoir des documents plus courts, plus simples et écrits dans un langage clair; ces changements pourraient rendre les publications du CEPMB plus claires et plus utiles pour tous les groupes d'intervenants.
- Élargir le public visé par les efforts de sensibilisation, mettre davantage l'accent sur les tiers payeurs et les groupes de défense des droits des patients. L'évaluation a révélé qu'un certain nombre de répondants issus des catégories de défense des droits des patients et des tiers payeurs ignoraient la nature des renseignements et des analyses que produit le CEPMB et désiraient être mieux informés.
|
|
Plans en vue de donner suite à la priorité
Accélérer les processus du CEPMB
- Mettre en œuvre les Règles de pratique et de procédure révisées aux fins des audiences.
- Réaliser les objectifs de rendement pour les processus et les procédures choisis.
- Raccourcir le délai de production des rapports.
- Améliorer l'efficacité du processus de consultation auprès des principaux intervenants nommés dans la Loi au moyen de processus plus informels.
Simplifier davantage les Lignes directrices
- Continuer d'évaluer l'application et l'incidence des modifications apportées aux Lignes directrices par l'intermédiaire du Plan de surveillance et d'évaluation des principales modifications aux Lignes directrices, présenter au Conseil une mise à jour annuelle et publier les constatations sur le site Web du CEPMB.
- Effectuer une analyse de la méthodologie de rajustement du prix selon l'IPC pour déterminer s'il pourrait être avantageux d'apporter des modifications.
- Faire le suivi de l'issue des contrôles judiciaires afin de mettre au clair les questions relatives à la réglementation et tenir compte des résultats dans les Lignes directrices du Conseil, s'il y a lieu.
Encourager l'utilisation d'un langage clair dans les communications du CEPMB
- Continuer d'utiliser la version « En bref » du rapport annuel.
- Continuer d'utiliser les « résumés analytiques », qui ont récemment été lancés, pour mettre en évidence les constatations des études analytiques et leur incidence sur les politiques.
- Continuer d'utiliser les résumés dans tous les rapports du SNIUMP.
- Élaborer un guide sur la réglementation des prix qui explique le cadre réglementaire et le processus d'examen des prix.
Élargir le public visé par les efforts de sensibilisation
- Poursuivre la mise en œuvre de la politique d'engagement des intervenants non liés à l'industrie.
- Organiser et tenir une série de réunions bilatérales auprès des intervenants non liés à l'industrie.
- Faire le compte rendu du processus de traitement des plaintes des consommateurs dans le rapport annuel du CEPMB.
|
| Priorité |
Type |
Résultats stratégiques et (ou) programmes |
| Réduction du fardeau réglementaire et utilisation efficace des ressources du personnel du Conseil |
Déjà établie |
Liens aux programmes 1 et 2 |
| Description |
|
Pourquoi s'agit-il d'une priorité?
En janvier 2011, le premier ministre a lancé la Commission sur la réduction de la paperasse (CRP) dans le cadre du Plan d'action économique. La Commission a été invitée à cerner les irritants pour les entreprises, dont les effets sont manifestement néfastes pour la croissance, la concurrence et l'innovation, et à recommander des moyens de s'y attaquer et de réduire le fardeau lié à la conformité de façon durable, tout cela devant être assuré sans compromettre la protection de l'environnement ou la santé et la sécurité des Canadiens.
Il a été établi ultérieurement que les irritants désignés par l'industrie ne relevaient pas de la portée de cette initiative et qu'ils ne figuraient pas dans le rapport de la Commission. Le CEPMB espère néanmoins renforcer l'esprit de cette initiative en revoyant son processus d'examen des prix, afin de cerner des moyens possibles de réduire le fardeau réglementaire imposé aux brevetés, sans porter atteinte à son mandat de protection des consommateurs.
Par ailleurs, en conséquence des mesures de compression des dépenses prévues dans le budget de 2010, dans le cadre desquelles les budgets de fonctionnement des ministères ont été gelés à leurs niveaux de 2010-2011, le CEPMB a désigné des postes qui vont demeurer vacants. Il a ainsi mis en place une certaine efficacité opérationnelle qui pourra éventuellement être améliorée, afin d'assurer l'utilisation optimale des ressources.
|
|
Plans en vue de donner suite à la priorité
- Examiner la faisabilité d'une transition vers la présentation par les brevetés d'un seul rapport réglementaire par année sur les médicaments brevetés existants.
- Effectuer une analyse de la méthodologie de rajustement du prix selon l'Indice du prix à la consommation (IPC) du CEPMB.
- Évaluer les modifications que l'on pourrait apporter aux critères justifiant la tenue d'une enquête sur le prix d'un médicament breveté.
- Envisager des options permettant d'utiliser plus efficacement les ressources du personnel du Conseil par l'intermédiaire d'une initiative de planification de la relève et de transfert des connaissances.
|
Analyse des risques
Le Conseil d'examen du prix des médicaments brevetés (CEPMB) est un organisme indépendant qui détient des pouvoirs quasi judiciaires. Il a été créé par le Parlement en 1987 en vertu de la Loi sur les brevets (Loi).
Le Conseil est composé d'au plus cinq membres siégeant à temps partiel, dont un président et un vice-président. Tous les membres du Conseil sont nommés par le gouverneur en conseil. En vertu de la Loi sur les brevets, le président du Conseil assume également les fonctions de chef de la direction et, en cette qualité, est chargé de la gouverne et de la supervision des activités du CEPMB.
Les membres du Conseil sont responsables de la mise en œuvre des dispositions applicables de la Loi. Ensemble, ils établissent les Lignes directrices, les règles, les règlements administratifs et les autres politiques du Conseil, comme le prévoit la Loi et consultent au besoin des intervenants, y compris les ministres de la Santé et les représentants de groupes de consommateurs, l'industrie pharmaceutique et d'autres personnes et, au besoin, tiennent des audiences.
Les nominations au Conseil sont recommandées au Bureau du Conseil privé par la ministre de la Santé. En ce moment, un des cinq postes au Conseil est vacant. Le nombre insuffisant de membres du Conseil peut avoir une incidence sur la célérité du processus d'audience. Il est important pour le Conseil d'avoir une combinaison appropriée de compétences. La présidente continuera de fournir à la ministre de la Santé des recommandations adaptées aux compétences nécessaires pour faire partie du Conseil.
À l'heure actuelle, un certain nombre de décisions prises par le Conseil issues des audiences font l'objet d'un contrôle judiciaire. Bien que les décisions judiciaires présentent un risque, elles offrent aussi aux brevetés et au personnel du Conseil la possibilité d'obtenir des précisions sur les dispositions législatives et réglementaires importantes et sur l'application des Lignes directrices connexes du Conseil. Le Conseil continuera de faire le suivi des décisions judiciaires se rapportant à ces instances.
Les dépenses liées aux soins de santé continuent d'augmenter dans la plupart des pays industrialisés, selon l'Organisation de coopération et de développement économiques (OCDE). La plupart des pays industrialisés, dont le Canada, ont des programmes et des systèmes de médicaments subventionnés par l'État qui réglementent, de diverses manières, les prix des médicaments ou les profits des fabricants de médicaments pour tenter de limiter la hausse du coût des médicaments.
Selon l'Institut canadien d'information sur la santé, les dépenses liées aux médicaments représentent la deuxième part en importance des dépenses totales de santé, après les dépenses des hôpitaux. Au cours des dernières années, le prix élevé des nouveaux produits médicamenteux brevetés, plus particulièrement celui des produits biologiques présentant des indications ultérieures, a soulevé des questions concernant le besoin de soumettre ces nouvelles indications à des examens de prix supplémentaires. Par l'intermédiaire du Plan de surveillance et d'évaluation des principales modifications aux Lignes directrices et grâce au travail qu'il effectue auprès de représentants des régimes d'assurance-médicaments fédéraux, provinciaux et territoriaux, le Conseil continuera de faire le suivi des enjeux liés à son mandat de réglementation.
En tant qu'organe d'experts fédéral en matière de prix des médicaments, le CEPMB, par l'intermédiaire de son Programme sur les tendances relatives aux produits pharmaceutiques, contribue à la prise de décisions éclairées en faisant rapport des tendances relatives aux prix des produits pharmaceutiques. Par les analyses critiques des tendances relatives aux prix, à l'utilisation et aux coûts des médicaments qu'il effectue en vertu de l'initiative du Système national d'information sur l'utilisation des médicaments prescrits (SNIUMP), le CEPMB fournit au système des soins de santé canadien une mine de renseignements complets et précis sur l'utilisation faite des médicaments d'ordonnance et les facteurs de coûts. Pour le CEPMB, la difficulté consiste à s'assurer que ses rapports fournissent des renseignements pertinents et qu'ils sont publiés en temps utile, de façon à procurer des renseignements crédibles sur les tendances relatives aux prix des produits pharmaceutiques et à répondre aux besoins d'information des différents décideurs en matière de politique.
Les activités menées par le CEPMB dans le cadre de l'initiative du SNIUMP ont été entreprises en vertu d'un protocole d'entente (PE) entre Santé Canada et le CEPMB. Santé Canada et le CEPMB évaluent de temps à autre ce PE et peuvent y mettre un terme ou modifier ses dispositions à la lumière de futurs besoins budgétaires ou stratégiques.
En tant qu'organisme de petite taille, le CEPMB arrive difficilement à recruter et à conserver des spécialistes hautement qualifiés dans leur domaine. Le CEPMB éprouve actuellement des difficultés à trouver des candidats possédant les compétences nécessaires pour mener des analyses économiques quantitatives. Qui plus est, dans les prochains 12 à 36 mois, des personnes occupant des postes clés dans d'autres directions de l'organisme seront admissibles à la retraite. Ces postes nécessitent souvent différentes compétences utilisées de façon intermittente, ce qui complique le transfert des connaissances et crée des défis pour l'organisme. L'année 2013-2014 offrira l'occasion, et le défi, de s'assurer que la planification de la relève soutient les besoins organisationnels en évolution et les orientations de la politique opérationnelle. Cela comprendra la formation du personnel par l'intermédiaire d'un programme d'affectation et de formation polyvalente visant à développer les ensembles de compétences requis au sein de l'organisme. Le CEPMB travaillera aussi à déterminer d'autres façons de trouver des personnes possédant les compétences nécessaires.
En dernier lieu, le gouvernement a présenté un certain nombre d'initiatives pangouvernementales, comme Services partagés Canada, l'Initiative des normes de service, la transformation de la gestion financière et le projet de Processus opérationnels communs des ressources humaines. Ces initiatives engendrent des défis pour tous les ministères, parce qu'elles ont une incidence sur la charge de travail et les ressources. Le CEPMB continuera à travailler de concert avec les organismes centraux et les autres types d'organismes, comme le Réseau des administrateurs de petits organismes, pour appuyer ces initiatives de la façon qui s'impose compte tenu de sa taille et pour tirer profit des ententes conclues au sein de ce regroupement de petits organismes.
Sommaire de la planification
Ressources financières (dépenses prévues en milliers de dollars)
Total des dépenses budgétaires (Budget principal des dépenses)
2013-2014 |
Dépenses prévues3 2013–2014 |
Dépenses prévues 2014–2015 |
Dépenses prévues 2015–2016 |
|
3 Les dépenses prévues pour 2013-2014 comprennent un report estimatif d'environ 234,5 milliers de dollars.
|
| 10 944,1 |
11 178,6 |
10 902,6 |
10 902,6 |
Ressources humaines (équivalents temps plein – ETP)
| 2013–2014 |
2014–20154 |
2015–2016 |
|
4 On a déterminé qu'en raison des gains en efficience réalisés grâce à d'autres initiatives, le CEPMB était en mesure d'éliminer un poste sans que cela n'ait d'incidence sur ses activités.
|
| 74 |
73 |
73 |
Tableau récapitulatif de la planification pour les programmes (en milliers de dollars)
| Résultat stratégique |
Programme |
Dépenses réelles 2010–2011 |
Dépenses réelles 2011–2012 |
Dépenses projetées 2012–20135 |
Dépenses prévues |
Harmonisation avec les résultats du gouvernement du Canadaii |
2013-
20146 |
2014-
2015 |
2015-
2016 |
|
5 Il est prévu dans les dépenses projetées pour 2012-2013 qu'un montant de 2 204,2 milliers de dollars provenant de l'affectation à but spécial ne sera pas dépensé à la fin de l'exercice relativement au Programme de réglementation du prix des médicaments brevetés.
6 Les dépenses prévues pour 2013-2014 comprennent l'entière somme de l'affectation à but spécial, soit 2 470,0 milliers de dollars.
|
| Les médicaments brevetés ne peuvent être vendus au Canada à des prix excessifs afin de protéger les intérêts de la population canadienne, et les intervenants sont tenus informés des tendances relatives aux produits pharmaceutiques. |
Le Programme de réglementation du prix des médicaments brevetés |
4 232,0 |
7 346,8 |
3 391,1 |
6 781,3 |
6 781,3 |
6 781,3 |
Des Canadiens en santé |
| Le Programme sur les tendances relatives aux produits pharmaceutiques |
890,4 |
1 010,5 |
899,8 |
1 328,8 |
1 287,4 |
1 287,4 |
Des Canadiens en santé |
| Total partiel |
5 122,4 |
8 357,3 |
4 290,9 |
8 110,1 |
8 068,7 |
8 068,7 |
|
Tableau récapitulatif de la planification pour les services internes (en milliers de dollars)
| Programme |
Dépenses réelles 2010-2011 |
Dépenses réelles 2011-2012 |
Dépenses projetées 2012-2013 |
Dépenses prévues |
| 2013–20147 |
2014–2015 |
2015–2016 |
| 7 Le report estimatif d'environ 234,5 milliers de dollars est inclus dans les dépenses prévues pour les Services internes. |
| Services internes |
4 348,3 |
3 397,1 |
2 838,5 |
3 068,4 |
2 833,9 |
2 833,9 |
| Total partiel |
4 348,3 |
3 397,1 |
2 838,5 |
3 068,4 |
2 833,9 |
2 833,9 |
Total du sommaire de la planification (en milliers de dollars)
| Résultat stratégique, programmes et services internes |
Dépenses réelles 2010-2011 |
Dépenses réelles 2011-2012 |
Dépenses projetées 2012-2013 |
Dépenses prévues |
| 2013–20148 |
2014–2015 |
2015–2016 |
| 8 Le total des dépenses prévues pour 2013-2014 comprend un report estimatif d'environ 234,5 milliers de dollars. |
| Total |
9 470,7 |
11 754,4 |
7 129,4 |
11 178,6 |
10 902,6 |
10 902,6 |
Profil des dépenses
Tendances au chapitre des dépenses ministérielles
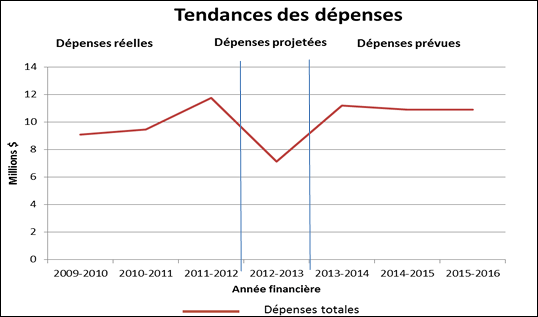
Tendances au chapitre des dépenses ministérielles
Le graphique linéaire simple qui suit montre la tendance en matière de dépenses du CEPMB. Il illustre les dépenses réelles des exercices 2009-2010, 2010-2011 et 2011-2012, les dépenses projetées pour l'exercice 2012-2013 et les dépenses prévues pour les exercices 2013-2014, 2014-2015 et 2015-2016.
Afin de pouvoir affronter les pressions découlant de la charge de travail et de poursuivre les activités en cours liées à l'exercice de son mandat, le Conseil du Trésor a autorisé le CEPMB à augmenter les niveaux de référence au crédit 45 (Dépenses de programme) de 5,6 millions de dollars pour 2009-2010, de 6,2 millions de dollars pour 2010-2011 et de 5,8 millions de dollars pour 2011-2012 et les années ultérieures (dont le régime d'avantages sociaux des employés [RASE], exception faite des frais des locaux de Travaux publics et Services gouvernementaux Canada [TPSGC]).
Le CEPMB a maintenant achevé la dotation de tous les postes prévus et prévoit que ses dépenses réelles (à l'exception de l´affectation à but spécial) tiendront compte du financement accordé en 2013-2014 et pour les années ultérieures.
Dans le cadre de cette augmentation du financement, on a autorisé 2,2 millions de dollars en 2009-2010 et 2,8 millions de dollars en 2010-2011 et pour les années ultérieures aux fins de l'affectation à but spécial (ABS) réservée pour la tenue d'audiences publiques. Le financement permanent total de l'ABS a donc augmenté à 3,1 millions de dollars. L'ABS ne peut être utilisé que pour couvrir les coûts liés à la tenue d'audiences publiques.
Quand se tiennent des audiences, en moyenne 90 % des dépenses provenant de l'ABS sont affectées aux frais des services juridiques et des témoins experts. Ces frais dépendent entièrement du nombre d'audiences tenues de même que de la durée et de la complexité des audiences, et sont donc très difficiles à prévoir. Pour cette raison, les fonds de l'ABS qui ne sont pas requis pour la tenue d'audiences sont retournés au Trésor. Au cours des dernières années, le Conseil a délivré moins d'Avis d'audiences et, par conséquent, on s'attend à ce que les fonds de l'ABS ne soient pas entièrement utilisés pendant cette période de planification.
Suite aux mesures de limitation des coûts prévues au budget fédéral de 2010, les budgets de fonctionnement ministériels ont été gelés aux niveaux de 2010-2011 pour 2011-2012 et 2012-2013.
De plus, le budget de 2012 a permis des économies de 1 million de dollars, réalisées par suite d'une réduction de 144 000 milliers de dollars du financement accordé au Programme sur les tendances relatives aux produits pharmaceutiques et d'une réduction de 630 000 milliers de dollars du financement accordé à l'ABS, qui est inclus dans le financement accordé au Programme d'examen du prix des médicaments brevetés. Le financement accordé au Programme sur les tendances relatives aux produits pharmaceutiques a davantage reculé de 167 milliers de dollars pour 2013-2014 et de 63 milliers de dollars pour 2014-2015 et les années ultérieures.
Budget des dépenses par crédit voté
Pour obtenir plus de renseignements sur nos crédits organisationnels, veuillez consulter la page 162 du Budget principal des dépenses de 2013-2014iii.
Section II : Analyse des programmes par résultat stratégique
Résultat stratégique
| Résultat stratégique : Les médicaments brevetés ne peuvent être vendus au Canada à des prix excessifs afin de protéger les intérêts de la population canadienne, et les intervenants sont tenus informés des tendances relatives aux produits pharmaceutiques. |
| Indicateurs de rendement |
Objectifs |
| Au Canada, les prix des médicaments brevetés se situent dans la fourchette des prix pratiqués dans les sept pays de comparaison nommés dans le Règlement. |
Au Canada, les prix des médicaments brevetés se situent au niveau ou sous la médiane des prix internationaux |
Programmes
Deux programmes viennent appuyer l'unique résultat stratégique du CEPMB :
- le Programme de réglementation du prix des médicaments brevetés;
- le Programme sur les tendances relatives aux produits pharmaceutiques.
Programme 1 : Le Programme de réglementation du prix des médicaments brevetés
Le Conseil d'examen du prix des médicaments brevetés (CEPMB) est un organisme indépendant qui détient des pouvoirs quasi judiciaires et qui est responsable de s'assurer que les prix auxquels les brevetés vendent leurs médicaments brevetés au Canada ne sont pas excessifs en vertu des facteurs d'examen du prix prévus à la Loi sur les brevets (la Loi). Pour décider si un prix est excessif, le Conseil doit tenir compte des facteurs suivants : les prix de vente du médicament et des autres médicaments de la même catégorie thérapeutique au Canada et dans les sept pays de comparaison nommés dans le Règlement sur les médicaments brevetés (le Règlement); les variations de l'Indice des prix à la consommation (IPC); et, conformément à la Loi, tous les autres facteurs précisés par les règlements d'application visant l'examen du prix. En vertu de la Loi et du Règlement, les brevetés sont tenus de faire rapport des renseignements sur les prix et les ventes pour chaque médicament breveté vendu au Canada, jusqu'à échéance du brevet ou des brevets. Le personnel du Conseil examine les renseignements soumis par les brevetés au lancement et à chaque période de rapport, et ce, pour tous les médicaments brevetés vendus au Canada. S'il conclut que le prix d'un médicament breveté semble excessif, le personnel du Conseil mène une enquête sur le prix. Une enquête peut se solder par un des résultats suivants : la fermeture de l'enquête lorsqu'il apparaît que le prix est non excessif; un Engagement de conformité volontaire par lequel le breveté s'engage à réduire le prix de son produit et à rembourser les recettes excessives au moyen d'un paiement et (ou) d'une réduction du prix d'un autre produit médicamenteux breveté; ou une audience publique dont l'objet est de déterminer si le prix du produit médicamenteux est ou non excessif, y compris une ordonnance corrective rendue par le Conseil. Si le Panel d'audience du Conseil conclut, à l'issue d'une audience publique, qu'un prix est ou était excessif, il peut ordonner au breveté de réduire le prix et de prendre des mesures qui lui sont dictées pour rembourser les recettes excessives. Ce programme assure la protection des Canadiens et de leur système des soins de santé en effectuant l'examen des prix auxquels les brevetés vendent leurs médicaments brevetés au Canada afin d'éviter les prix excessifs.
Ressources financières (en milliers de dollars)
Total des dépenses budgétaires (Budget principal des dépenses)
2013-2014 |
Dépenses prévues
2013-2014 |
Dépenses prévues
2014-2015 |
Dépenses prévues
2015-2016 |
| 6 781,3 |
6 781,3 |
6 781,3 |
6 781,3 |
Ressources humaines (ETP)
| 2013–2014 |
2014–2015 |
2015–2016 |
| 44 |
44 |
44 |
| Programme Résultats attendus |
Indicateurs de rendement |
Objectifs |
| La conformité des brevetés à la Loi sur les brevets, à la réglementation et aux Lignes directrices sur les prix excessifs (les Lignes directrices) |
Pourcentage de médicaments brevetés dont les prix sont fixés en conséquence de la conformité volontaire, suivant les Lignes directrices ou ne justifient pas la tenue d'une enquête |
Les prix de 95 % des médicaments brevetés sont volontairement fixés suivant les Lignes directrices ou ne justifient pas la tenue d'une enquête. |
| Pourcentage de médicaments brevetés faisant l'objet d'une ordonnance du Conseil |
Les ordonnances du Conseil sont intégralement respectées. |
Faits saillants de la planification
Il incombe au CEPMB de s'assurer que les prix départ-usine, soit les prix auxquels les brevetés vendent leurs médicaments brevetés au Canada pour usage humain ou usage vétérinaire, ne sont pas excessifs. Dans la mesure du possible, le Conseil compte sur la conformité volontaire, cette méthode étant plus rapide et plus économique pour toutes les parties. La conformité volontaire des brevetés est facilitée par l'intermédiaire des Lignes directrices publiées, qui ont pour objet d'aider les brevetés à établir des prix qui ne sont pas excessifs en leur fournissant des renseignements transparents et prévisibles sur la conduite de l'examen des prix.
Depuis la mise en œuvre des nouvelles Lignes directrices en janvier 2010, le personnel du Conseil surveille et évalue de façon continue l'application et l'incidence des principales modifications apportées. En juin 2011, le CEPMB a publié son Plan de surveillance et d'évaluation des principales modifications aux Lignes directrices et, en décembre 2011, a réalisé la première évaluation annuelle en vertu du plan. Il est possible que cette incidence ne soit pas d'emblée évidente en raison du calendrier de présentation des rapports réglementaires des brevetés, du processus d'examen des prix des médicaments brevetés établi en fonction d'une année civile complète, et du fait que plusieurs périodes de rapport peuvent s'avérer nécessaires avant que l'on puisse percevoir des tendances. Néanmoins, le Conseil surveillera les nouveaux enjeux afin de repérer le besoin d'apporter d'autres modifications aux Lignes directrices ou au Plan de surveillance.
Au cours de la période de planification, les principales priorités quant au Programme de réglementation du prix des médicaments brevetés (réglementation des prix) sont les suivantes :
- Continuer de surveiller et d'évaluer l'incidence des nouvelles Lignes directrices.
- Accélérer les processus du CEPMB de la façon suivante :
- mettre en œuvre les Règles de pratique et de procédure révisées aux fins des audiences;
- établir des objectifs de rendement pour les processus et les procédures choisis, le cas échéant;
- améliorer l'efficacité du processus de consultation au moyen de procédures plus informelles.
- Simplifier davantage les Lignes directrices de la façon suivante :
- effectuer une analyse de la méthodologie de rajustement du prix selon l'IPC pour déterminer s'il pourrait être avantageux d'apporter des modifications;
- faire le suivi de l'issue des contrôles judiciaires afin de préciser les questions relatives à la réglementation et tenir compte des résultats dans les Lignes directrices du Conseil, s'il y a lieu.
- Encourager l'utilisation d'un langage clair dans toutes les publications du CEPMB de la façon suivante :
- élaborer un guide sur la réglementation des prix qui explique les fondements du régime de réglementation et la façon dont il fonctionne.
- Réduire le fardeau réglementaire et faire un usage efficace des ressources du personnel du Conseil de la façon suivante :
- examiner la faisabilité de la transition de deux rapports réglementaires à un seul rapport réglementaire par année pour les médicaments brevetés existants;
- évaluer le caractère adéquat des critères actuels justifiant la tenue d'une enquête.
- Envisager des options permettant une utilisation plus efficace des ressources du personnel du Conseil par l'intermédiaire de l'initiative de planification de la relève et de transfert des connaissances.
Avantages pour les Canadiens
Cette activité de programme contribue au résultat recherché par le gouvernement du Canada qui est de favoriser la santé de la population canadienne, en s'assurant que les prix auxquels sont vendus les médicaments brevetés au Canada ne sont pas excessifs. Les examens de prix, les enquêtes et, lorsqu'il y a lieu, les audiences, doivent être menés avec transparence, de façon efficace et dans des délais raisonnables, de manière à protéger les intérêts des consommateurs et du système canadien de soins de santé.
Programme 2 : Le Programme sur les tendances relatives aux produits pharmaceutiques
Le CEPMB rend annuellement compte au Parlement, par le truchement du ministre de la Santé, de ses activités d'examen du prix, des prix des médicaments brevetés et des tendances observées au niveau des prix de tous les médicaments ainsi que des dépenses de R-D rapportées par les brevetés pharmaceutiques. À l'appui de cette exigence en matière de rapport, le Programme sur les tendances relatives aux produits pharmaceutiques fournit des renseignements complets et précis sur les tendances relatives aux prix auxquels les fabricants vendent leurs médicaments brevetés au Canada et sur les dépenses de recherche-développement des brevetés aux intervenants intéressés, notamment l'industrie (c.-à-d. de médicaments de marque, issus de la biotechnologie et génériques); les gouvernements fédéral, provinciaux et territoriaux; les groupes de défense des droits des consommateurs et des patients; les tiers payants; et autres. Ces renseignements permettent également de rassurer les Canadiens que les prix des médicaments brevetés ne sont pas excessifs. De plus, suivant l'établissement du Système national d'information sur l'utilisation des médicaments prescrits (SNIUMP) par les ministres de la Santé fédéral, provinciaux et territoriaux, le ministre de la Santé a demandé au CEPMB d'effectuer des analyses des tendances relatives au prix, à l'utilisation et aux coûts des médicaments d'ordonnance afin de s'assurer que le système canadien de soins de santé possède des renseignements complets et précis sur l'utilisation des médicaments d'ordonnance et sur les facteurs à l'origine des augmentations de coûts. Le CEPMB publie des rapports du SNIUMP particuliers fondés sur les priorités en matière de recherche et de rapport cernées par le Comité directeur du SNIUMP.
Ressources financières (en milliers de dollars)
Total des dépenses budgétaires (Budget principal des dépenses)
2013-2014 |
Dépenses prévues
2013-2014 |
Dépenses prévues
2014-2015 |
Dépenses prévues
2015-2016 |
| 1 328,8 |
1 328,8 |
1 287,4 |
1 287,4 |
Ressources humaines (ETP)
| 2013–2014 |
2014–2015 |
2015–2016 |
| 11 |
10 |
10 |
| Programme Résultats attendus |
Indicateurs de rendement |
Objectifs |
| Les intervenants sont plus conscients des tendances relatives aux produits pharmaceutiques de même que des facteurs de coût. |
Nombre d'appels de fichier |
Augmentation de 5 % du nombre de demandes |
| Nombre de présentations organisées par le CEPMB dans le cadre de réunions externes |
10 événements par année |
Faits saillants de la planification
Le CEPMB continuera, en menant les activités suivantes, de présenter des rapports pertinents et en temps utile, de fournir des renseignements crédibles sur les tendances relatives aux produits pharmaceutiques et de répondre aux besoins d'information de divers décideurs :
- Rendre annuellement compte au Parlement, par le truchement du ministre de la Santé, de ses principales activités, de ses activités d'examen du prix, des prix des médicaments brevetés et des tendances observées au niveau des prix de tous les médicaments ainsi que des dépenses de R-D rapportées par les brevetés pharmaceutiques.
- Répondre aux besoins d'information des gouvernements FPT cernés par le Comité directeur du SNIUMP.
- Encourager l'utilisation d'un langage clair dans toutes les communications du CEPMB :
- Continuer d'utiliser la version « En bref » du rapport annuel.
- Continuer d'utiliser les « résumés analytiques », qui ont récemment été lancés, pour mettre en évidence les constatations des études analytiques et leur incidence sur les politiques.
- Continuer d'utiliser les résumés dans tous les rapports du SNIUMP.
- Fournir en temps utile les résultats d'études analytiques pertinentes menées en vertu de l'initiative du SNIUMP.
Avantages pour les Canadiens
Cette activité de programme contribue au résultat recherché par le gouvernement du Canada qui est de favoriser la santé de la population canadienne, en présentant des analyses critiques des tendances relatives aux prix, à l'utilisation et aux coûts des médicaments brevetés, afin que le système canadien des soins de santé dispose de renseignements plus complets et plus précis pour éclairer la prise de décisions stratégiques sur les médicaments.
Services internes
Les Services internes sont des groupes d'activités et de ressources connexes gérés de façon à répondre aux besoins des programmes et des autres obligations générales d'une organisation. Ces groupes sont les suivants : services de gestion et de surveillance, services des communications, services juridiques, services de gestion des ressources humaines, services de gestion financière, services de gestion de l'information, services des technologies de l'information, services des biens immobiliers, services du matériel, services des acquisitions, et services de voyages et autres services administratifs. Les Services internes comprennent uniquement les activités et les ressources destinées à l'ensemble d'une organisation et non celles fournies à un programme particulier.
Ressources financières (en milliers de dollars)
Total des dépenses budgétaires (Budget principal des dépenses)
2013-2014 |
Dépenses prévues9
2013–2014 |
Dépenses prévues
2014–2015 |
Dépenses prévues
2015–2016 |
| 9 Le report estimatif d'environ 234,5 milliers de dollars est inclus dans les dépenses prévues pour les Services internes. |
| 2 833,9 |
3 068,4 |
2 833,9 |
2 833,9 |
Ressources humaines (ETP)
| 2013–2014 |
2014–2015 |
2015–2016 |
| 19 |
19 |
19 |
Section III : Renseignements supplémentaires
Principales données financières
États financiers prospectifs
Les faits saillants des états financiers prospectifs inclus dans ce RPP visent à offrir une vue d'ensemble de la situation financière et des activités du CEPMB. Ces faits saillants des états financiers prospectifs sont établis selon la méthode de la comptabilité d'exercice afin de renforcer la responsabilisation et d'améliorer la transparence et la gestion financière.
Les états financiers prospectifsiv du CEPMB sont affichés sur son site Web à l'adresse http://www.pmprb-cepmb.gc.ca, sous la rubrique « Rapports au Parlement ».
État consolidé prospectif des activités et de la situation financière nette de l'organisme (non vérifié)
Pour l'exercice s'étant terminé le 31 mars 2013 |
|
% Variation |
Prévisions 2013-2014 |
Résultats estimatifs 2012-2013 |
| Total des dépenses |
50 % |
12 083 054 $ |
8 058 202 $ |
| Total des revenus |
(100 %) |
0 |
(26 004 613) |
| Coût de fonctionnement net avant le financement du gouvernement et les transferts |
1 673 % |
12 083 054 $ |
(17 946 411 $) |
Total des dépenses : Le Conseil d'examen du prix des médicaments brevetés prévoit des dépenses de 12,1 millions de dollars selon le Budget principal des dépenses de 2013-2014 et les renseignements sur les obligations. Ce montant ne comprend pas le Budget supplémentaire des dépenses. Cette différence de 4,0 millions de dollars par rapport aux prévisions pour 2012-2013 ne représente pas une hausse réelle des affectations budgétaires, qui sont identiques à celles indiquées dans le sommaire de la planification. La différence de 4,0 millions de dollars prévoit des dépenses de l'entière somme de l'affectation à but spécial (ABS), soit 2,5 millions de dollars, et supporte en outre toutes les dépenses des sommes votées et statutaires accordées au CEPMB en 2013-2014. Pour de plus amples renseignements sur l'ABS, veuillez consulter le Profil des dépenses.
Les dépenses par activité de programme sont réparties comme suit : 7,4 millions de dollars pour le Programme de réglementation du prix des médicaments brevetés; 1,5 millions de dollars pour le Programme sur les tendances relatives aux produits pharmaceutiques; et 3,2 millions de dollars pour les Services internes, y compris les indemnités de vacances et les congés compensatoires de même que les avantages sociaux futurs.
Total des revenus : Les recettes non disponibles constituent les sommes déclarées à titre de revenus. Les sommes comptabilisées dans les recettes non disponibles ne représentent pas les recettes générées par le CEPMB. Ce sont plutôt les sommes que les brevetés ont versées au gouvernement du Canada en application des modalités d'un Engagement de conformité volontaire ou d'une ordonnance du Conseil aux fins de rembourser les recettes excessives. Le ministre peut conclure avec toute province des ententes concernant le partage avec celle-ci de sommes versées par les brevetés au receveur général, déduction faite des frais de perception et de partage. Les recettes non disponibles sont réalisées pour le compte du gouvernement.
État consolidé prospectif de la situation financière (non vérifié)
Pour l'exercice s'étant terminé le 31 mars 2013 |
| (en dollars) |
%
Variation |
Prévisions
2013-2014 |
Résultats estimatifs
2012-2013 |
| Total du passif net |
(4 %) |
1 704 981 $ |
1 769 934 $ |
| Total des actifs financiers nets |
(0 %) |
779 176 |
781 133 |
| Dette nette du ministère |
(6 %) |
925 805 $ |
988 801 $ |
| Position financière nette du ministère |
(6 %) |
(925 805) |
(988 801) |
Passif par catégorie : Le total du passif prévu est de 1,7 millions de dollars en 2013-2014, une baisse nette de 65,0 milliers de dollars par rapport aux prévisions pour 2012-2013.
Le passif est réparti comme suit : 3,6 millions de dollars pour les créditeurs et charges à payer; 259,0 milliers de dollars pour les indemnités de vacances et de congés compensatoires; et 691,0 milliers de dollars pour les indemnités de départs. On prévoit que les charges à payer détenus pour le compte du gouvernement seront de 2,8 millions de dollars.
Actif par catégorie : Le total de l'actif prévu est de 779,2 milliers de dollars en 2013-2014, une baisse de 2,0 milles de dollars par rapport aux prévisions pour 2012-2013.
Le montant à recevoir du Trésor prévu est de 624,4 milliers de dollars en 2013-2014, représentant une hausse de 11,9 milliers de dollars par rapport aux prévisions pour 2012-2013. On prévoit que les débiteurs et avances seront de 154,8 milliers de dollars. L'analyse des tendances indique que la variation nette des débiteurs et des avances de Conseil d'examen du prix des médicaments brevetés représentera une baisse de 13,8 milliers de dollars.
Liste des tableaux de renseignements supplémentaires
La version électronique de tous les tableaux de renseignements supplémentairesv qui figurent dans le Rapport sur les plans et les priorités de 2013-2014 est affichée sur le site Web du CEPMB à l'adresse http://www.pmprb-cepmb.gc.ca, sous la rubrique « Rapports au Parlement/Rapport sur les plans et les priorités ».
- Écologisation des opérations gouvernementales
- Sources des revenus disponibles et des revenus non disponibles
- Vérifications internes et évaluations à venir au cours des trois prochains exercices;
Rapport sur les dépenses fiscales et les évaluations
Il est possible de recourir au régime fiscal pour atteindre des objectifs de la politique publique en appliquant des mesures spéciales, comme de faibles taux d'imposition, des exemptions, des déductions, des reports et des crédits. Le ministère des Finances publie annuellement des estimations et des projections du coût de ces mesures dans son rapport intitulé Dépenses fiscales et évaluationsvi. Les mesures fiscales présentées dans le rapport Dépenses fiscales et évaluations relèvent de la responsabilité exclusive du ministre des Finances.
Section IV : Autres sujets d'intérêt
Coordonnées de la personne-ressource de l'organisme
Le Conseil d'examen du prix des médicaments brevetés
Case L40
Centre Standard Life
333, avenue Laurier Ouest
Bureau 1400
Ottawa (Ontario) K1P 1C1
Téléphone : 613-952-7360
Sans frais : 1-877-861-2350
Télécopieur : 613-952-7626
ATS : 613-957-4373
Courriel : pmprb@pmprb-cepmb.gc.ca
Site Web : www.pmprb-cepmb.gc.ca
Renseignements supplémentaires
Rapport annuel 2011 du CEPMB
Publication trimestrielle La Nouvelle
Guide du breveté
Compendium des politiques, des Lignes directrices et des procédures – Mise à jour : juin 2012
Loi sur les brevets
Règlement sur les médicaments brevetés
Notes en fin d'ouvrage
- Pour de plus amples renseignements sur l'initiative du Système national d'information sur l'utilisation des médicaments prescrits (SNIUMP), veuillez consulter le site Web du CEPMB : http://www.pmprb-cepmb.gc.ca, sous la rubrique « SNIUMP ».
- Pour des renseignements sur la correspondance de la contribution des ministères avec les résultats du gouvernement du Canada, veuillez consulter le site Web du Secrétariat du Conseil du Trésor (http://www.tbs-sct.gc.ca/ppg-cpr/frame-cadre-fra.aspx).
- Pour obtenir plus de renseignements sur nos crédits organisationnels, veuillez consulter le Budget principal des dépenses de 2013-2014 sur le site Web du Secrétariat du Conseil du Trésor à l'adresse http://www.tbs-sct.gc.ca/ems-sgd/esp-pbc/me-bpd-fra.asp .
- Les états financiers prospectifs du CEPMB sont affichés sur son site Web, sous la rubrique « Rapports au Parlement », à l'adresse http://www.pmprb-cepmb.gc.ca/CMFiles/Reports%20to%20Parliament/Future%20Oriented%20Financial%20Statements%20Final%20Signed.pdf (en anglais).
- La version électronique de tous les tableaux de renseignements supplémentaires qui figurent dans le Rapport sur les plans et les priorités de 2013-2014 est affichée sur le site Web du CEPMB : www.pmprb-cepmb.gc.ca.
- Le rapport annuel intitulé Dépenses fiscales et évaluations se trouve sur le site Web du ministère des Finances à l'adresse http://www.fin.gc.ca/purl/taxexp-fra.asp