Rapport ministériel sur le rendement 2013-2014
Conseil d’examen du prix des médicaments brevetés
L’honorable Rona Ambrose
Ministre de la Santé
Nombre de catalogue : H79-2/2014F-PDF
ISSN : 2368-1071
Table des matières
Avant-propos
Message de la présidente
Section I : Vue d’ensemble des dépenses de l’organisation
Section II : Analyse des programmes par résultat stratégique
Section III : Renseignements supplémentaires
Section IV : Coordonnées de l’organisation
Annexe : Définitions
Notes de fin de document
Avant-propos
Le rapport ministériel sur le rendement fait partie de la série de documents budgétaires. Ces documents appuient les lois de crédits, qui précisent les montants pouvant être dépensés par le gouvernement et à quelles fins générales. Les documents budgétaires comptent trois parties.
Partie I – Le Plan de dépenses du gouvernement présente un aperçu des dépenses fédérales.
Partie II – Le budget principal des dépenses décrit les ressources financières requises au prochain exercice pour chaque ministère, organisme et société d’État.
Partie III – Les plans de dépenses des ministères sont constitués de deux documents. Le rapport sur les plans et les priorités (RPP) est un plan de dépenses établi par chaque ministère et organisme qui reçoit des crédits parlementaires (à l’exception des sociétés d’État). Ce rapport présente des renseignements détaillés, pour une période de trois ans commençant à l’exercice indiqué dans le titre du rapport, sur les priorités, les résultats stratégiques, les programmes, les résultats attendus et les ressources connexes requises. Le Rapport ministériel sur le rendement (RMR) dresse un bilan du rendement réel obtenu par chaque ministère et organisme au cours du plus récent exercice terminé, en fonction des plans, des priorités et des résultats attendus énoncés dans son propre RPP. Le RMR informe les parlementaires et la population des résultats obtenus par les organisations pour les Canadiens.
Le budget supplémentaire des dépenses renferme en outre des renseignements sur les besoins relatifs aux dépenses qui n’étaient pas suffisamment définis pour être inclus dans le budget principal des dépenses ou qui ont ultérieurement été précisés afin de rendre compte de l’évolution de programmes et de services donnés.
L’information financière présentée dans le RMR provient directement des autorisations décrites dans le budget principal des dépenses et des renseignements fournis dans le RPP sur les dépenses prévues. Cette information financière correspond à celle fournie dans les Comptes publics du Canada. Ceux ci renferment l’État consolidé de la situation financière, l’État consolidé des résultats et du déficit accumulé, l’État consolidé de la variation de la dette nette et l’État consolidé des flux de trésorerie du gouvernement du Canada, de même que des renseignements détaillés des opérations financières ventilés par portefeuille ministériel pour un exercice donné. Deux types d’information financière présentée dans le RMR proviennent des Comptes publics du Canada : les autorisations budgétaires disponibles pour emploi au nouvel exercice par une organisation qui reçoit des crédits parlementaires, et les autorisations utilisées lors de cet exercice. Ces dernières autorisations correspondent aux dépenses réelles décrites dans le RMR.
La Politique sur la structure de la gestion, des ressources et des résultats du Conseil du Trésor favorise une plus grande concordance de l’information sur le rendement présentée dans les RMR, les autres documents budgétaires et les Comptes publics du Canada. Pour les organisations qui reçoivent des crédits parlementaires, la Politique définit l’architecture d’alignement des programmes comme une structure par rapport à laquelle l’information sur le rendement financier et non financier est fournie aux fins des documents budgétaires et des rapports au Parlement. Peu importe si l’organisation présente l’information dans le budget principal des dépenses, le RPP, le RMR ou les Comptes publics du Canada, la même structure est utilisée.
Dans le but de mieux appuyer les décisions sur les crédits, un certain nombre de changements ont été apportés aux RMR en 2013-2014. Le RMR présente maintenant les renseignements sur les finances, les ressources humaines et le rendement dans la section II, au niveau le plus bas de l’architecture d’alignement des programmes, le cas échéant.
Le format et la terminologie du RMR ont également été modifiés afin de le rendre plus clair et cohérent et de mettre davantage l’accent sur l’information du budget des dépenses et des Comptes publics. De plus, l’information ministérielle concernant la Stratégie fédérale de développement durable (SFDD) a été regroupée dans un nouveau tableau de renseignements supplémentaires qui sera affiché sur le site Web du ministère. Ce tableau comprend tous les éléments de la Stratégie qui étaient auparavant fournis dans les RMR et les sites Web ministériels, y compris les rapports sur l’écologisation des opérations gouvernementales et les évaluations environnementales stratégiques. La section III du rapport fournira un lien vers le nouveau tableau dans le site Web du ministère. Enfin, les définitions des termes utilisés sont maintenant fournies en annexe.
Message de la présidente
C’est avec plaisir que je vous présente le Rapport ministériel sur le rendement 2012-2013 du Conseil d’examen du prix des médicaments brevetés (CEPMB).
L’objectif du CEPMB de s’assurer que les Canadiens ne paient pas un prix trop élevé pour des médicaments brevetés est d’une grande importance qui contribue au but général du gouvernement du maintien de la santé des Canadiens.
Au cours du dernier exercice, le CEPMB s’est efforcé avant tout d’améliorer ses programmes en surveillant l’effet qu’exercent les modifications apportées aux Lignes directrices et de publier des études qui expliquent les plus récentes tendances du marché et rendent compte des intérêts immédiats des payeurs publics et privés. Le CEPMB a également poursuivi ses activités de communication, étendu et diversifié les échanges qu’il a avec ses intervenants. En outre, il a joué un rôle plus actif après de ses partenaires fédéraux, provinciaux et internationaux et s’est davantage impliqué avec eux.
Fidèle à l’esprit du Plan d’action sur la réduction du fardeau administratif du gouvernement, le Conseil a mené à bon terme les consultations sur deux initiatives destinées à alléger le fardeau imposé par la réglementation. En premier lieu, il a simplifié la méthodologie de rajustement du prix selon l’Indice des prix à la consommation (IPC), et il mettra la méthodologie simplifiée en œuvre en 2015. En second lieu, le Conseil a proposé des modifications au Règlement sur les médicaments brevetés i afin de ramener la fréquence de dépôt de semestrielle à annuelle. Le travail est en cours pour la publication préalable des modifications proposées du Règlement dans la partie I de la Gazette du Canada aux fins de consultation officielle en 2014-2015.
Trois décisions du Conseil ont fait l’objet d’un contrôle judiciaire par la Cour fédérale : ratio-Salbutamol HFA (T-1058-11; T-1825-11); ratiopharm Inc. (à présent Teva Canada) (T-1252-11); et Sandoz Canada Inc. (T-161612). La Cour a entendu ces affaires en novembre 2013 et a rendu ses décisions le 27 mai 2014. La Cour fédérale a admis les demandes de contrôle judiciaire et a renvoyé les affaires au Conseil en l’instruisant de trouver que ratiopharm Inc. et Sandoz Canada Inc. ne sont pas des brevetés aux fins de l’article 79 de la Loi sur les brevets et que ces entreprises ne relèvent pas de ce fait de la compétence du Conseil. Le Bureau du Procureur général a déposé des avis d’appel de ces décisions le 25 juin 2014.
Malgré les nouveaux défis et les problèmes qui se font jour, le CEPMB continue de faire passer la protection des intérêts des consommateurs avant tout, en reconnaissant cependant la valeur que les médicaments novateurs offrent aux patients. Ceci n’est rendu possible que grâce aux efforts menés en collaboration par les membres et le personnel du Conseil et à leur dévouement.
Mary Catherine Lindberg
Présidente
Section I : Vue d’ensemble des dépenses de l’organisation
Profil de l’organisation
Ministre de tutelle : L’honorable Rona Ambrose
Premier dirigeant : Mary Catherine Lindberg, Présidente
Portefeuille ministériel : Santé
Instruments habilitants : Loi sur les brevetsii et Règlement sur les médicaments brevetésiii
Année d’incorporation ou de création : 1987
Autre : Le ministre de la Santé est responsable de l’application des dispositions de la Loi sur les brevets (la Loi) formulées aux articles 79 à 103. Le Conseil d’examen du prix des médicaments brevetés (CEPMB) fait partie du portefeuille de la Santé, qui est également constitué de Santé Canada, de l’Agence de la santé publique du Canada, des Instituts de recherche en santé du Canada et de l’Agence canadienne d’inspection des aliments. Le portefeuille de la Santé aide le ministre de la Santé à maintenir et à améliorer la santé des Canadiens.
Même s’il fait partie du portefeuille de la Santé, le CEPMB exerce son mandat en toute indépendance vis-à-vis du ministre de la Santé. Le CEPMB fonctionne également d’une façon indépendante des autres organismes, à savoir Santé Canada, qui autorise la vente des médicaments au Canada après avoir vérifié leur innocuité, leur efficacité et leur qualité; les régimes publics fédéral, provinciaux et territoriaux d’assurance-médicaments qui autorisent l’inscription des médicaments sur leurs formulaires de médicaments admissibles à un remboursement; et le Programme commun d’examen des médicaments, géré par l’Association canadienne des médicaments et des technologies de la santé (ACMTS), qui évalue l’efficience des médicaments avant leur inscription sur les formulaires des régimes publics d’assurance-médicaments participants.
Contexte organisationnel
Raison d’être
Créé par le Parlement en 1987, le Conseil d’examen du prix des médicaments brevetés (CEPMB) est un organisme indépendant qui détient des pouvoirs quasi judiciaires. Il est investi d’un double mandat :
- Réglementation – Veiller à ce que les prix auxquels les brevetés vendent leurs médicaments brevetés au Canada ne soient pas excessifs.
- Rapport – Faire rapport des tendances des prix de tous les médicaments ainsi que des dépenses des brevetés dans la R-D au Canada.
Dans l’exécution de son mandat, le CEPMB veille à la protection des Canadiens en s’assurant que les médicaments brevetés ne sont pas vendus au Canada à des prix excessifs et que les intervenants sont tenus informés des tendances relatives aux produits pharmaceutiques.
Responsabilités
Le CEPMB a été créé en 1987 par suite de la modification à la Loi sur les brevets (la Loi), le projet de loi C-22. La Loi a été modifiée à nouveau en 1993 (projet de loi C-91), afin de renforcer ses pouvoirs d’apporter des recours. Les révisions s’inscrivaient dans des réformes réglementaires visant à établir un juste équilibre entre les mesures de protection des brevets visant à encourager les efforts de recherche et développement des brevetés pharmaceutiques et la nécessité de protéger les intérêts des consommateurs.
Le CEPMB a un double mandat :
Réglementation du prix des médicaments brevetés
Il incombe au CEPMB de s’assurer que les prix départ-usine, à savoir les prix auxquels les brevetés vendent, au Canada, à leurs différents clients (grossistes, hôpitaux, pharmacies et autres) leurs médicaments brevetés pour usage humain ou pour usage vétérinaire distribués sous ordonnance ou en vente libre, ne sont pas excessifs. Le CEPMB réglemente le prix de chaque médicament breveté auquel Santé Canada a attribué un numéro d’identification du médicament (DIN) dans le cadre de son processus d’examen. Le mandat du Conseil couvre également les médicaments distribués au titre du Programme d’accès spécial ou distribués en vertu du programme d’essais cliniques de même que les drogues nouvelles de recherche. Les prix des médicaments brevetés en vente libre et les médicaments brevetés à usage vétérinaire sont également réglementés par le Conseil en fonction des plaintes reçues.
Dans le cas où, à l’issue d’une audience publique, le Conseil juge que le prix d’un médicament breveté vendu sur un marché canadien est ou était excessif, il peut rendre une ordonnance obligeant le breveté à réduire le prix de son médicament et à appliquer les mesures qui lui sont dictées pour rembourser les recettes excessives qu’il a tirées de la vente de son médicament à un prix excessif.
Rapport sur les tendances relatives aux produits pharmaceutiques
Chaque année, le CEPMB rend compte au Parlement, par le truchement du ministre de la Santé, de ses principales activités, de ses analyses du prix des médicaments brevetés et des tendances relatives aux produits pharmaceutiques d’ordonnance ainsi que des dépenses de R-D déclarées par les sociétés pharmaceutiques détentrices de brevets. De plus, par suite de l’établissement du Système national d'information sur l'utilisation des médicaments prescritsiv (SNIUMP) par les ministres fédéraux/provinciaux/territoriaux (F/P/T) de la Santé, la ministre de la Santé, en vertu des pouvoirs qui lui sont conférés par l’article 90 de la Loi sur les brevets, a demandé au CEPMB de mener une analyse sur les prix, l’utilisation et les tendances liées aux coûts de médicaments d’ordonnance brevetés et non brevetés, pour que le système de santé du Canada ait des renseignements plus complets et plus justes sur l’utilisation de tous les médicaments d’ordonnance et les sources des hausses de prix. Cette fonction vise à aider les gouvernements F/P/T et d'autres parties intéressées à se munir d’une source centralisée d’information crédible sur les tendances dans l’industrie pharmaceutique.
Résultats stratégiques et architecture d’alignement des programmes
1. Résultat stratégique : Les médicaments brevetés ne peuvent être vendus au Canada à des prix excessifs, afin de protéger les intérêts de la population canadienne. La population canadienne est également tenue informée.
1.1 Programme : Le programme de réglementation du prix des médicaments brevetés
1.2 Programme : Le programme sur les tendances relatives aux produits pharmaceutiques
Services internes
Priorités organisationnelles
| Priorité |
Type 1 |
Résultat stratégique [et/ou] programmes |
| Poursuivre la mise en œuvre du plan d’action de la direction donnant suite au Rapport d’évaluation des programmes du CEPMB |
Déjà établie |
Liens aux programmes 1 et 2 |
| Sommaire des progrès |
|
Quels progrès ont été réalisés à l’égard de cette priorité?
Le plan d’action de la direction donnant suite au Rapport d’évaluation des programmes du CEPMB devait aborder les quatre sujets de réflexion signalés au Conseil.
Accélérer les processus du CEPMB
Mettre en œuvre des objectifs de rendement pour des processus/procédures sélectionnés
- Les résultats en matière de rendement du CEPMB par rapport aux normes de service sont mesurés au courant de l’année civile, parce que les dépôts d’information qu’il reçoit reposent sur de l’information sur les prix et les ventes pour une année civile.
- Les résultats en matière de rendement pour l’année civile 2013 pour chacune des normes de service suivantes sont affichés sur son site Web :
- La norme de service pour l’examen scientifique des nouveaux produits médicamenteux brevetésv – établit le délai pour l’expédition de rapports émanant du Groupe consultatif sur les médicaments pour usage humain (GCMUH) au breveté
- La norme de service pour l’examen du prix des nouveaux produits médicamenteux brevetésvi – établit les délais pour la communication des résultats de l’examen des prix pour les nouveaux produits médicamenteux brevetés
- La norme de service pour l’examen du prix des produits médicamenteux brevetés existantsvii – établit les délais pour la présentation du formulaire 2 et la communication des résultats de l’examen des prix pour les produits médicamenteux brevetés
Amélioration de l’opportunité des rapports
Le CEPMB a constitué un groupe de travail inter-directions afin d’apprendre à mieux comprendre les facteurs qui déterminent les tendances signalées dans son Rapport annuel et le Plan de surveillance et d’évaluation des lignes directrices (PSELD). Les travaux du groupe permettront d’amplifier l’information dont dispose le Conseil pour prendre des décisions et de faciliter une surveillance plus proactive des tendances pertinentes.
En outre, le CEPMB projette de tenir un forum de chercheurs en août 2014 dans le cadre de l’initiative du SNIUMP. L’objectif de ce forum de chercheurs consiste à avoir un échange d’information avec les principaux universitaires travaillant dans le domaine de la recherche économique pharmaceutique et de la politique fondée sur des données probantes. Le forum permettra d’échanger de l’information sur les prochains travaux de recherche qui seront menés pas le SNIUMP et sur le travail que les chercheurs qui y participent entreprennent. Le forum servira à rehausser le profil des travaux du SNIUMP et à nouer des relations de pair à pair avec les principaux leaders d’opinion dans le domaine. Les résultats du forum serviront également à déterminer de futures priorités en matière de recherche pour le SNIUMP.
En 2013-2014, le CEPMB, dans le cadre de l’initiative du SNIUMP, a publié cinq rapports :
Simplifier davantage les Lignes directrices
Continuer d’évaluer l’application et l’incidence des modifications apportées aux Lignes directrices
- En décembre 2013, le personnel du Conseil a présenté la troisième évaluation annuelle dans le cadre du Plan de surveillance et d’évaluation des principales modifications aux Lignes directrices, 2013 (GMEP 2013)xiii au Conseil. Les résultats du GMEP pour les trois dernières années sont disponibles sur le site Web du CEPMB sous Loi et règlement.
- Le Conseil a examiné les commentaires présentés au sujet de l’Avis et commentaires d’octobre 2013 concernant l’initiative relative à la Méthodologie de rajustement du prix selon l’IPC. Le Conseil a approuvé la méthodologie de rajustement du prix selon l’IPC retardé, laquelle remplacera la méthodologie de rajustement du prix selon l’IPC prévu en utilisant un IPC réel dans le calcul du facteur de rajustement du prix selon l’IPC pour la période de prévision. Cette nouvelle méthodologie de rajustement retardé du prix selon l’IPC sera mise en œuvre le 1er janvier 2015.
Encourager l’utilisation d’un langage clair dans les communications du CEPMB
Tous les rapports du SNIUMP diffusés en 2013-2014 comprenaient un résumé.
Élargir le public visé par les efforts de sensibilisation
En 2013, le CEPMB a continué d’améliorer la sensibilisation de ses intervenants non industriels au moyen d’échanges bilatéraux avec les représentants en santé F-P-T, les tiers payants et d’autres groupes. En outre, le CEPMB a commencé à travailler à l’organisation d’un forum des chercheurs dans le cadre de l’initiative du SNIUMP. L’objectif du forum des chercheurs consiste à avoir un échange d’information avec les principaux universitaires travaillant dans le domaine de la recherche économique pharmaceutique et de la politique fondée sur des données probantes. Le CEPMB s’est également joint au réseau Pharmaceutical Pricing and Reimbursement Information (PPRI). Le réseau PPRI est une initiative de réseautage et de partage d’information de l’Organisation mondiale de la Santé sur des questions d’établissement de prix et de remboursement des produits pharmaceutiques. Le réseau PPRI est composé de plus de 60 membres, principalement des instances compétentes et des tiers payants de 38 pays au total.
|
| Priorité |
Type |
Résultat stratégique [et/ou] programmes |
| Réduction du fardeau réglementaire et utilisation efficace des ressources du personnel du Conseil |
Déjà établie |
Liens aux programmes 1 et 2 |
| Sommaire des progrès |
|
Quels progrès ont été réalisés à l’égard de cette priorité?
Examiner la faisabilité d’une transition vers la présentation par les brevetés d’un seul rapport réglementaire par année sur les médicaments brevetés existants.
Le CEPMB met en œuvre une initiative afin d’assouplir les exigences relatives aux rapports que doivent produire les brevetés.
Effectuer une analyse de la méthodologie de rajustement du prix selon l’Indice du prix à la consommation (IPC) du CEPMB
Le Conseil a révisé les commentaires reçus dans le cadre de la consultation sur la méthodologie de rajustement du prix selon l’IPC retardé en octobre 2013. Le Conseil a approuvé la méthodologie de rajustement du prix selon l’IPC retardé, laquelle remplacera la méthodologie de rajustement du prix selon l’IPC prévu en utilisant un IPC réel dans le calcul du facteur de rajustement du prix selon l’IPC pour la période de prévision. Cette nouvelle méthodologie de rajustement retardé du prix selon l’IPC sera mise en œuvre le 1er janvier 2015.
Envisage des options permettant d’utiliser plus efficacement les ressources du personnel du Conseil par l’intermédiaire d’une initiative de planification de la relève et de transfert des connaissances
En 2012-2013, le CEPMB a embauché un expert-conseil et l’a chargé d’entreprendre une consultation exhaustive avec les principaux membres du personnel, d’organiser des forums dans lesquels les employés peuvent partager des expériences et des défis du leadership, ainsi que d’effectuer une analyse approfondie de la structure actuelle de l’organisation. Le rapport, qui a été terminé au début de 2013-2014, a fourni des éléments de réflexion qui portaient principalement sur le perfectionnement du personnel, la planification de la relève et d’éventuels changements de l’aménagement organisationnel.
Perfectionnement du personnel
- En 2013-2014, le CEPMB a donné à ses employés accès au perfectionnement des compétences et au transfert de connaissances en leur proposant un certain nombre d’affectations de perfectionnement (affectations par intérim et échanges de postes entre directions).
Planification de la relève
- Le CEPMB a effectué une analyse du profil des principaux postes des membres de l’équipe de la haute direction. On a acquis une compréhension fondamentale des défis qui découleront à l’avenir des départs à la retraite prévus et planifiés et d’éventuelles vacances de poste clés à court et à long terme.
|
Principaux risques
| Risques |
Stratégie d’atténuation du risque |
Lien à l’architecture d’alignement des programmes |
| Une pénurie de membres du Conseil peut influer sur l’opportunité du processus d’audience et le mélange de compétences approprié |
En juillet 2014, le cinquième membre du Conseil a été nommé. L’effectif de membres du CEPMB est désormais complet. |
1.1 – Le programme de réglementation du prix des médicaments brevetés |
| L’évolution des médicaments brevetés dans des domaines plus complexes et plus novateurs risque d’entraver la capacité du CEPMB à s’acquitter efficacement de son mandat |
Le Conseil continue d’évaluer et d’examiner d’éventuelles modifications de ses Lignes directrices afin qu’elles demeurent efficaces sur le plan de l’exécution de son mandat et de la promotion de la conformité volontaire de la part des brevetés. |
1.1 – Le programme de réglementation du prix des médicaments brevetés |
| Résultats défavorables de contrôles judiciaires |
Le CEPMB examine à l’heure actuelle l’incidence que pourraient avoir deux récentes décisions de la Cour fédérale au sujet de la compétence du Conseil à l’égard de certains médicaments génériques. |
1.1 – Le programme de réglementation du prix des médicaments brevetés |
| Présentation de rapports périmés et non pertinents |
En 2013-2014, le CEPMB s’est de plus en plus attaché à des stratégies destinées à améliorer l’efficacité et la pertinence de son mandat en matière de présentation de rapports. La parution de rapports réguliers sera normalisée et annoncée à l’avance dans le programme de recherche du SNIUMP. Pour garantir la pertinence des rapports du SNIUMP, le CEPMB a lancé une stratégie d’engagement plus vaste afin de déterminer les priorités en matière de recherche et les domaines d’intérêt émergents. Le CEPMB a intensifié ses efforts de communication avec les principaux intervenants, parmi lesquels des universitaires, les partenaires fédéraux du portefeuille de la santé, les collectivités gouvernementales chargées de l’élaboration de politiques et de la recherche, l’industrie pharmaceutique et de l’assurance ainsi que les professionnels de la santé, les groupes de défense des patients et des consommateurs. |
1.2 – Le programme sur les tendances relatives aux produits pharmaceutiques |
| Difficulté d’attirer et de retenir des experts en la matière hautement spécialisés |
Le CEPMB élabore un plan d’action à partir du rapport de 2013-2014 sur la planification de la relève. Il augmente également la rémunération versée aux membres du Groupe consultatif sur les médicaments pour usage humain (GCMUH) afin de la rendre plus concurrentiel avec celle qui est versée par d’autres organismes publics pour du travail semblable. |
1.1 – Le programme de réglementation du prix des médicaments brevetés
1.2 – Le programme sur les tendances relatives aux produits pharmaceutiques |
Le Conseil est constitué d’au maximum cinq membres qui siègent à temps partiel, parmi lesquels un président et un vice-président. Le président est désigné en vertu de la Loi comme chef de la direction du CEPMB, revêtu de l’autorité et de la responsabilité de superviser et de diriger ses travaux.
Il incombe aux membres du Conseil de mettre en œuvre les dispositions en vigueur de la Loi. Ils établissent d’un commun accord les lignes directrices, les règles, les statuts et d’autres politiques du Conseil prévues par la Loi et consultent au besoin les intervenants, parmi lesquels le ministre de la Santé et les représentants de groupes de consommateurs, de l’industrie pharmaceutique et des gouvernements provinciaux et territoriaux et tiennent des audiences lorsque cela s’impose.
Les nominations au Conseil sont recommandées au Bureau du Conseil privé par le ministre de la Santé. En juillet 2014, un cinquième membre a été nommé, ce qui fait qu’à présent le CEPMB a son plein effectif de membres.
Ces dernières années, le prix élevé et l’utilisation de nouveaux produits pharmaceutiques brevetés, en particulier des produits biologiques comportant de nouvelles indications, ont fait naître des questions au sujet de la nécessité d’effectuer ultérieurement des examens supplémentaires des prix de ces produits. Au moyen de son Plan de surveillance et d’évaluation des lignes directrices et du travail qu’il effectue avec les représentants des régimes d’assurance-médicaments F-P-T et d’autres intervenants, le Conseil approfondira son étude de ces questions.
En 2015, le CEPMB mettra en œuvre une nouvelle méthodologie de rajustement du prix selon l’IPCxiv qui remplacera la méthodologie de rajustement du prix selon l’IPC prévu en utilisant un IPC réel dans le calcul du facteur de rajustement du prix selon l’IPC pour la période de prévision.
Le 27 mai 2014, la Cour fédérale a rendu ses décisions au sujet de demandes de contrôle judiciaire de deux décisions prises par le Conseil à la suite d’audiences. Dans les deux cas, la Cour fédérale a statué que l’entreprise n’était pas un « breveté » au sens de l’article 79 de la Loi et que, par conséquent, elle ne relevait pas de la compétence du Conseil. Bien que les décisions de la Cour posent un risque, elles procurent également l’occasion de fournir des éclaircissements aux brevetés et au personnel du Conseil au sujet des principales dispositions de la Loi et du règlement et de l’application des Lignes directrices connexes du Conseil. Le Procureur général a déposé des avis d’appel de ces décisions le 25 juin 2014.
En tant qu’organisme fédéral expert sur les questions afférentes au prix des médicaments, le CEPMB, par le biais du Programme sur les tendances relatives aux produits pharmaceutiques, concourt à la prise de décisions éclairées en faisant rapport des tendances relatives aux produits pharmaceutiques. En outre, le CEPMB entreprend des études et effectue des analyses sur divers sujets qui ont trait à l’établissement des prix et aux coûts des produits pharmaceutiques. Au moyen d’analyses critiques sur les tendances relatives aux prix, à l’utilisation et aux coûts, effectuées dans le cadre de l’initiative SNIUMP, le CEPMB fournit au système de santé du Canada de l’information exhaustive et exacte sur la façon dont les médicaments d’ordonnance sont utilisés et sur les déterminants des coûts. En 2013-2014, le CEPMB s’est de plus en plus attaché à des stratégies destinées à améliorer l’efficacité et la pertinence de son mandat en matière de présentation de rapports. La parution de rapports réguliers sera normalisée et annoncée à l’avance dans le programme de recherche du SNIUMP. Pour garantir que les rapports du SNIUMP soient pertinents, le CEPMB s’est lancé dans une vaste stratégie d’engagement afin de déterminer les priorités en matière de recherche et les domaines d’intérêt émergents. Le CEPMB a intensifié ses efforts de communication avec les principaux intervenants, parmi lesquels des universitaires, les partenaires fédéraux du portefeuille de la santé, les collectivités gouvernementales chargées de l’élaboration de politiques et de la recherche, l’industrie pharmaceutique et de l’assurance ainsi que les professionnels de la santé, les groupes de défense des patients et des consommateurs. En 2013-2014, le CEPMB a diffusé cinq nouvelles études.
Conformément à la directive sur la gestion du rendement du CT, le CEPMB s’est engagé à maintenir une culture de haut rendement. En mars 2014, le CEPMB a commencé à mettre en place un programme de gestion du rendement des employés comportant des évaluations du rendement annuelles écrites de tous les employés; les examens de milieu d’année commenceront en 2014-2015. Le CEPMB a également entrepris un examen de sa politique de reconnaissance des employés et la révisera au besoin afin de répondre aux nouvelles exigences du gouvernement. En outre, le CEPMB s’est engagé à mettre en place un plan de gestion des talents qui documente les possibilités d’apprentissage et les affectations grâce auxquelles un employé peut favoriser son avancement professionnel et accroître sa responsabilité. Le CEPMB a déjà lancé des initiatives destinées à améliorer le perfectionnement de ses employés grâce à des affectations internes et des programmes de transfert de formation afin de doter l’organisation de l’ensemble de compétences dont elle a besoin, et il a également intégré la planification de la relève à ses travaux de planification des activités.
Dépenses réelles
Ressources financières budgétaires (dollars)
Budget principal des
dépenses 2013-2014 |
Dépenses prévues
2013-2014 |
Autorisations totales
pouvant être utilisées
2013-2014 |
Dépenses réelles
(autorisations utilisées)
2013-2014 |
Écart (dépenses
réelles moins
dépenses prévues) |
| 10 944 073 |
11 178 573 |
*14 235 359 |
10 540 567 |
(638 006) |
* L’écart entre le Budget principal des dépenses et les Autorisations totales pouvant être utilisées est en grande partie imputable au financement supplémentaire reçu au moyen d’un mandat de rajustement pour couvrir le montant que la Cour fédérale a ordonné de rembourser à un breveté. La Cour fédérale a annulé une ordonnance du Conseil et ordonné dans sa décision qu’un revenu excédentaire de 2 801 285 $ soit remboursé par le CEPMB au breveté, avec l’intérêt approprié et les frais déterminés.
Le Budget principal des dépenses et les Autorisations totales pouvant être utilisées comprennent 2 470 000 $ dans une affectation à but spécial (ABS). L’ABS ne peut être utilisée que pour couvrir les coûts des audiences publiques, notamment les avocats externes, des témoins experts, etc. Tout montant non dépensé est reversé au Fonds du Trésor (le Trésor). En 2013-2014, les dépenses au titre de l’ABS s’élevaient à 60 641 $.
|
Ressources humaines (équivalents temps plein [ETP])
Prévu
2013-2014 |
Réel
2013-2014 |
Écart (réel moins prévu)
2013-2014 |
| 74,0 |
55,4 |
(18,6) |
| Le CEPMB a déterminé qu’à la suite de gains d’efficacité réalisés grâce à diverses initiatives, il était en position de laisser quelques postes vacants sans que cela touche considérablement ses opérations pour l’instant. |
Sommaire du rendement budgétaire pour les résultats stratégiques et les programmes (dollars)
| Résultats stratégiques, programmes et Services internes |
Budget principal des dépenses 2013-2014 |
Dépenses prévues 2013-2014 |
Dépenses prévues 2014-2015 |
Dépenses prévues 2015-2016 |
Autorisations totales pouvant être utilisées 2013-2014 |
Dépenses réelles (autorisations utilisées) 2013-2014 |
Dépenses réelles (autorisations utilisées) 2012-2013 |
Dépenses réelles (autorisations utilisées) 2011-2012 |
| Résultat stratégique 1 : Les médicaments brevetés ne peuvent être vendus au Canada à des prix excessifs, afin de protéger les intérêts de la population canadienne. La population canadienne est également tenue informée. |
| Le programme de réglementation du prix des médicaments brevetés |
*6 781 301 |
6 781 301 |
6 827 010 |
6 827 010 |
9 669 981 |
**6 395 602 |
3 888 795 |
7 346 773 |
| Total partiel |
6 781 301 |
6 781 301 |
6 827 010 |
6 827 010 |
9 669 981 |
6 395 602 |
3 888 795 |
7 346 773 |
| Le programme sur les tendances relatives aux produits pharmaceutiques |
1 328 833 |
1 328 833 |
1 267 557 |
1 267 557 |
1 314 847 |
1 146 790 |
983 279 |
1 010 528 |
| Total partiel |
1 328 833 |
1 328 833 |
1 267 557 |
1 267 557 |
1 314 847 |
1 146 790 |
983 279 |
1 010 528 |
Services internes
Total partiel |
2 833 939 |
3 068 439 |
2 832 463 |
2 832 463 |
3 250 531 |
2 998 175 |
3 184 729 |
3 397 074 |
| Total |
10 944 073 |
11 178 573 |
10 927 030 |
10 927 030 |
14 235 359 |
10 540 567 |
8 056 803 |
11 754 375 |
* Le montant affecté dans le Budget principal des dépenses de 2013-2014 au Programme d’examen du prix des médicaments brevetés comprend des fonds de 2 470 000 $ destinés à l’ABS.
** Les dépenses réelles (autorisations utilisées) pour le Programme d’examen du prix des médicaments brevetés comprennent la somme de 2 801 285 $ plus l’intérêt approprié et les frais déterminés que la Cour fédérale a ordonné au CEPMB de rembourser au breveté lorsqu’elle a annulé l’ordonnance du Conseil.
|
Harmonisation des dépenses avec le cadre pangouvernemental
Harmonisation des dépenses réelles pour 2013-2014 avec le cadre pangouvernementalXV (dollars)
| Résultat stratégique |
Programme |
Secteur de dépenses |
Résultat du gouvernement du Canada |
Dépenses réelles 2013-2014 |
| Les médicaments brevetés ne peuvent être vendus au Canada à des prix excessifs, afin de protéger les intérêts de la population canadienne. La population canadienne est également tenue informée. |
1.1 Le programme de réglementation du prix des médicaments brevetés |
Affaires sociales |
Des Canadiens en santé |
6 395 602 |
| 1.2 Le programme sur les tendances relatives aux produits pharmaceutiques |
Affaires sociales |
Des Canadiens en santé |
1 146 790 |
Total des dépenses par secteur de dépenses (dollars)
| Secteur de dépenses |
Total des dépenses prévues |
Total des dépenses réelles |
| Affaires économiques |
|
|
| Affaires sociales |
8 110 134 |
7 542 392 |
| Affaires internationales |
|
|
| Affaires gouvernementales |
|
|
Tendances relatives aux dépenses du ministère
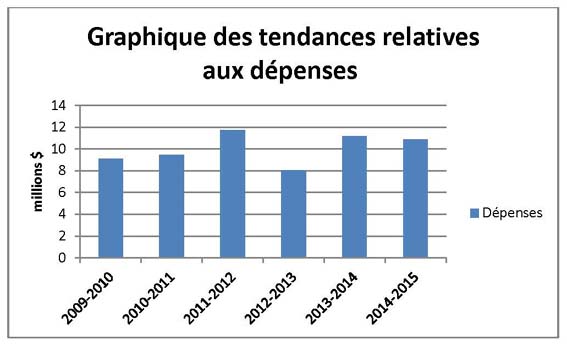
Les dépenses réelles de 2011–2012 sont considérablement plus élevées que les dépenses de l’exercice 2012-2013, parce que la Cour fédérale a annulé une décision du Conseil et a ordonné au CEPMB de rembourser 2 559 800 $ versés à la Couronne à la suite d’une ordonnance du Conseil.
En 2012-2013, le CEPMB n’a pas utilisé environ 3 millions de dollars de fonds de l’ABS, qui servent, au besoin, à tenir des audiences publiques, ainsi que 776 000 $ de son budget de fonctionnement. Ces écarts comprennent les 774 milliers de dollars en économies réalisées au moyen de processus d’efficience et de rationalisation des opérations. En 2012-2013, les fonds totaux de l’ABS s’élevaient à 3,1 millions de dollars. En 2013-2014, les fonds totaux de l’ABS ont été réduits à 2 470 000 $. L’ABS ne peut être utilisée que pour couvrir les coûts des audiences publiques, notamment les avocats externes, les témoins experts, etc. Tout montant non utilisé est retourné au Trésor.
En 2013-2014, la Cour fédérale a annulé une décision du Conseil et a ordonné au CEPMB de rembourser au breveté 2 801 000 $ qui avaient été payés à la Couronne à la suite d’une ordonnance du Conseil.
Les dépenses prévues pour les années ultérieures sont fondées sur l’hypothèse que la totalité des fonds de l’ABS seront dépensés chaque exercice.
Budget des dépenses par crédit voté
Pour obtenir des renseignements au sujet des crédits votés et des dépenses législatives du Conseil d’examen du prix des médicaments brevetés, veuillez consulter les Comptes publics du Canada 2014 sur le site Web de Travaux publics et Services gouvernementaux Canadaxvi.
Section II : Analyse des programmes par résultat stratégique
Résultat stratégique :
Les médicaments brevetés ne peuvent être vendus au Canada à des prix excessifs, afin de protéger les intérêts de la population canadienne. La population canadienne est également tenue informée.
Mesure du rendement
| Indicateurs de rendement |
Cibles |
Résultats réels |
| Au Canada, les prix des médicaments brevetés se situent dans la fourchette des prix pratiqués dans les sept pays de comparaison nommés dans le Règlement. |
Au Canada, les prix des médicaments brevetés se situent au niveau ou sous la médiane des prix internationaux. |
Les prix canadiens sont légèrement inférieurs au ratio moyen des prix internationaux médians observés chez les pays de comparaison. |
Dans le rapport annuel, le CEPMB présente des statistiques détaillées qui comparent les prix des médicaments brevetés à l’étranger à leurs prix canadiens. Pendant de nombreuses années, le CEPMB a fait rapport des ratios moyens des prix étrangers par rapport aux prix canadiens en convertissant les prix étrangers en prix équivalents en dollars canadiens au moyen des taux de change du marché. (Plus particulièrement, les moyennes mobiles sur 36 mois des taux du marché qu’utilise habituellement le CEPMB en appliquant ses Lignes directrices.) En se concentrant sur les résultats obtenus en effectuant la conversion des devises au taux de change du marché, on constate que les prix canadiens demeurent en moyenne inférieurs aux prix internationaux médians (c.-à-d. un ratio de 1,06 à 1). Par la même occasion, à l’exception des ratios États-Unis-Canada, tous les ratios moyens de prix bilatéraux ont fortement baissé ces dernières années. Pour placer cette tendance dans une perspective historique, en 2005, les prix canadiens étaient, en moyenne, environ égaux ou inférieurs aux prix correspondants dans tous les pays comparateurs autres que l’Italie. En 2013, les prix canadiens étaient résolument supérieurs aux prix au R.-U., en France et en Italie, et quelque peu plus élevés que les prix en Suède et en Suisse. Comme les années précédentes, les prix déclarés pour les États-Unis étaient bien plus élevés que les prix au Canada ou dans n’importe quel autre pays comparateur.
Programme 1.1 : Le programme de réglementation du prix des médicaments brevetés
Description
Le Conseil d’examen du prix des médicaments brevetés (CEPMB) est un organisme indépendant qui détient des pouvoirs quasi judiciaires et qui est responsable de s’assurer que les prix auxquels les brevetés vendent leurs médicaments brevetés au Canada ne sont pas excessifs en vertu des facteurs d’examen du prix prévus à la Loi sur les brevets (la Loi). Pour décider si un prix est excessif, le Conseil doit tenir compte des facteurs suivants : les prix de vente du médicament et des autres médicaments de la même catégorie thérapeutique au Canada et dans les sept pays de comparaison nommés dans le Règlement sur les médicaments brevetés (le Règlement); les variations de l’Indice des prix à la consommation (IPC); et, conformément à la Loi, tous les autres facteurs précisés par les règlements d’application visant l’examen du prix. En vertu de la Loi et du Règlement, les brevetés sont tenus de faire rapport des renseignements sur les prix et les ventes pour chaque médicament breveté vendu au Canada, jusqu’à échéance du brevet ou des brevets. Le personnel du Conseil examine les renseignements soumis par les brevetés au lancement et à chaque période de rapport, et ce, pour tous les médicaments brevetés vendus au Canada. S’il conclut que le prix d’un médicament breveté semble excessif, le personnel du Conseil mène une enquête sur le prix. Une enquête peut se solder par un des résultats suivants : la fermeture de l’enquête lorsqu’il apparaît que le prix est non excessif; un Engagement de conformité volontaire par lequel le breveté s’engage à réduire le prix de son produit et à rembourser les recettes excessives au moyen d’un paiement et (ou) d’une réduction du prix d’un autre produit médicamenteux breveté; ou une audience publique dont l’objet est de déterminer si le prix du produit médicamenteux est ou non excessif, y compris une ordonnance corrective rendue par le Conseil. Si le Panel d’audience du Conseil conclut, à l’issue d’une audience publique, qu’un prix est ou était excessif, il peut ordonner au breveté de réduire le prix et de prendre des mesures qui lui sont dictées pour rembourser les recettes excessives. Ce programme assure la protection des Canadiens et de leur système des soins de santé en effectuant l’examen des prix auxquels les brevetés vendent leurs médicaments brevetés au Canada afin d’éviter les prix excessifs.
Ressources financières budgétaires (dollars)
| Budget principal des dépenses 2013-2014 |
Dépenses prévues 2013-2014 |
Autorisations totales pouvant être utilisées 2013-2014 |
Dépenses réelles (autorisations utilisées) 2013-2014 |
Écart (dépenses réelles moins dépenses prévues) 2013-2014 |
| 6 781 301 |
6 781 301 |
9 669 981 |
6 395 602 |
(385 699) |
Ressources humaines (Équivalents temps plein [ETP])
| Prévu 2013-2014 |
Réel 2013-2014 |
Écart (nombre réel moins nombre prévu) 2013-2014 |
| 44,0 |
25,9 |
(18,1) |
| Le CEPMB a déterminé qu’à la suite de gains d’efficacité réalisés grâce à diverses initiatives, il était en position de laisser quelques postes vacants sans que cela touche considérablement ses opérations pour l’instant. |
Résultats du rendement
| Résultat attendu |
Indicateurs de rendement |
Cibles |
Résultats réels |
| La conformité des brevetés à la Loi sur les brevets, à la réglementation et aux Lignes directrices sur les prix excessifs (les Lignes directrices) |
Pourcentage de médicaments brevetés dont les prix sont fixés en conséquence de la conformité volontaire, suivant les Lignes directrices ou ne justifient pas la tenue d’une enquête. |
Les prix de 95 % des médicaments brevetés sont volontairement fixés suivant les Lignes directrices ou ne justifient pas la tenue d’une enquête. |
Les prix de 94,0 % des médicaments brevetés déclarés au CEPMB sont volontairement fixés suivant les Lignes directrices ou ne justifient pas la tenue d’une enquête. |
| Pourcentage de médicaments brevetés faisant l’objet d’une ordonnance du Conseil |
100 % des ordonnances du Conseil sont respectées. |
100 % des ordonnances du Conseil sont respectées. |
Analyse du rendement et leçons retenues
Les brevetés doivent veiller à ce que les prix des produits médicamenteux brevetés soient conformes aux Lignes directrices du Conseil pendant toutes les périodes pendant lesquelles les produits pharmaceutiques relèvent de la compétence du CEPMB.
En vertu des Lignes directrices, on donne l’occasion aux brevetés de présenter un Engagement de conformité volontaire lorsque le personnel du Conseil parvient à la conclusion, après avoir mené une enquête, que le prix d’un produit médicamenteux breveté vendu au Canada semble avoir dépassé les Lignes directrices. Un engagement de conformité volontaire peut également être présenté par un breveté après l’émission d’un avis d’audience. Un Engagement de conformité volontaire est un engagement écrit pris par un breveté de rajuster son prix afin de le rendre conforme aux Lignes directrices du Conseil.
En 2013, le personnel du Conseil a effectué des examens des prix de 1 341 des 1 343 médicaments brevetés nouveaux et existants vendus au Canada pour l’usage humain déclaré au CEPMB. En date du 31 mars 2014, deux médicaments brevetés étaient encore en cours d’examen. Sur le total des médicaments brevetés déclarés au CEPMB, le prix de 1 098 d’entre eux se situait à l’intérieur des lignes directrices et le prix de 164 autres n’a pas justifié la tenue d’une enquête – les prix de 94,0 % des médicaments brevetés sont volontairement fixés suivant les Lignes directrices ou ne justifient pas la tenue d’une enquête. Ceci est légèrement plus élevé que le chiffre de 92,5 % déclaré l’année dernière dans le RMR.
Depuis la mise en œuvre des nouvelles Lignes directrices en janvier 2010, le pourcentage de médicaments brevetés dont le prix est volontairement établi conformément aux Lignes directrices ou à un prix qui ne justifie pas la tenue d’une enquête a été supérieur à 90 % : 91,1 % en 2010; 94,6 % en 2011; 92,5 % en 2012 et 94,0 % en 2013.
Dans son rapport annuel de 2012, le CEPMB a commencé à déclarer le nombre d’Engagements de conformité volontaire acceptés par la présidente dans le tableau État d’avancement de l’examen du prix.
Lorsque le nombre d’Engagements de conformité volontaire est inclus comme élément du calcul du pourcentage de tous les médicaments brevetés déclarés au CEPMB dont le prix est volontairement établi conformément aux Lignes directrices ou à un prix qui ne justifie pas la tenue d’une enquête, le pourcentage de conformité volontaire passe de 92,5 % à 94,9 % en 2012, et de 94,0 % à 94,9 % en 2013.
Programme 1.2 : Le programme sur les tendances relatives aux produits pharmaceutiques
Description
Le CEPMB rend annuellement compte au Parlement, par le truchement du ministre de la Santé, de ses activités d’examen du prix, des prix des médicaments brevetés et des tendances observées au niveau des prix de tous les médicaments ainsi que des dépenses de R-D rapportées par les brevetés pharmaceutiques. À l’appui de cette exigence en matière de rapport, le Programme sur les tendances relatives aux produits pharmaceutiques fournit des renseignements complets et précis sur les tendances relatives aux prix auxquels les fabricants vendent leurs médicaments brevetés au Canada et sur les dépenses de recherche-développement des brevetés aux intervenants intéressés, notamment l’industrie (c.-à-d. de médicaments de marque, issus de la biotechnologie et génériques); les gouvernements fédéral, provinciaux et territoriaux; les groupes de défense des droits des consommateurs et des patients; les tiers payants; et autres. Ces renseignements permettent également de rassurer les Canadiens que les prix des médicaments brevetés ne sont pas excessifs. De plus, suivant l’établissement du Système national d’information sur l’utilisation des médicaments prescrits (SNIUMP) par les ministres de la Santé fédéral, provinciaux et territoriaux, le ministre de la Santé a demandé au CEPMB d’effectuer des analyses des tendances relatives au prix, à l’utilisation et aux coûts des médicaments d’ordonnance afin de s’assurer que le système canadien de soins de santé possède des renseignements complets et précis sur l’utilisation des médicaments d’ordonnance et sur les facteurs à l’origine des augmentations de coûts. Le CEPMB publie des rapports du SNIUMP particuliers fondés sur les priorités en matière de recherche et de rapport cernées par le Comité directeur du SNIUMP.
Ressources financières budgétaires (dollars)
| Budget principal des dépenses 2013-2014 |
Dépenses prévues 2013-2014 |
Autorisations totales pouvant être utilisées 2013-2014 |
Dépenses réelles (autorisations utilisées) 2013-2014 |
Écart (dépenses réelles moins dépenses prévues) 2013-2014 |
| 1 328 833 |
1 328 833 |
1 314 847 |
1 146 790 |
(182 043) |
Ressources humaines (Équivalents temps plein [ETP])
| Prévu 2013-2014 |
Réel 2013-2014 |
Écart (actual minus plannednombre réel moins nombre prévu) 2013-2014 |
| 11,0 |
7,2 |
(3,8) |
Résultats du rendement
| Résultat attendu |
Indicateurs de rendement |
Cibles |
Résultats réels |
| Les intervenants sont plus conscients des tendances relatives aux produits pharmaceutiques de même que des facteurs de coût. |
Nombre de visites du site Web |
Augmentation de 5 % du nombre de demandes/visites |
Non atteints |
| Nombre de présentations organisées par le CEPMB dans le cadre de réunions externes |
10 événements par année |
Participation à 26 événements extérieurs et présentation organisée à huit d’entre eux |
Analyse du rendement et leçons retenues
Les brevetés sont tenus, en vertu du Règlement, de présenter des renseignements détaillés sur les ventes de produits pharmaceutiques brevetés qu’ils réalisent, y compris les quantités vendues et les recettes nettes de chaque produit selon la catégorie de client dans chaque province/territoire. Le CEPMB utilise ces renseignements pour analyser les tendances des ventes, des prix et de l’utilisation de produits pharmaceutiques brevetés. (Des renseignements supplémentaires sur les résultats statistiques principaux de cette analyse se trouvent dans le Rapport annuel de 2013 du CEPMB qui est publié sur son site Web.)
En outre, la Loi charge le CEPMB de surveiller les dépenses de recherche-développement (R D) pharmaceutique et d’en faire rapport, sans conférer par règlement au CEPMB l’autorité d’examiner le montant ou le type des dépenses que les brevetés effectuent pour la recherche dans le contexte de sa réglementation des prix. (Des renseignements supplémentaires ayant trait aux principales statistiques sur l’état actuel de l’investissement dans la recherche pharmaceutique au Canada se trouvent dans le Rapport annuel de 2013 du CEPMB qui est publié sur son site Web.)
En 2013-2014, le CEPMB n’a pas atteint son objectif, en l’occurrence une augmentation de 5 % du nombre de visites de son site Web. Cependant, il a constaté une augmentation constante (59 % d’avril 2013 à mars 2014) du nombre de personnes qui le suivent sur Twitter.
Toutes les publications du CEPMB, y compris les études, les décisions du Conseil et les documents de référence, sont disponibles sur son site Web.
En 2013-2014, le CEPMB a organisé de nombreuses réunions avec des intervenants afin de les consulter au sujet de ses projets de recherche et de faire la promotion des résultats de ses études, notamment l’Association canadienne du médicament générique, l’Association des pharmaciens du Canada, l’Agence canadienne des médicaments et des technologies de la santé (ACMTS), l’Association canadienne du diabète et l’Association canadienne des compagnies d’assurances de personnes. En outre, le CEPMB a participé à 26 événements extérieurs et a présenté des exposés sur divers sujets à huit de ces événements. Les événements s’adressaient à des publics divers, notamment les principaux intervenants du CEPMB : brevetés, provinces, tiers payeurs et groupes de défense des patients.
Le CEPMB continue d’utiliser les nouveaux supports de communication, notamment les vidéoconférences et les webinaires, pour atteindre un plus grand nombre d’intervenants. En avril 2013, le CEPMB a organisé six webinaires pour la diffusion des résultats de son étude du SNIUMP intitulée L’utilisation de bandelettes de test glycémique dans certains régimes publics d’assurance-médicaments de 2008.
Le Système national d’information sur l’utilisation des médicaments prescrits (SNIUMP) est une initiative de recherche établie par les ministres de la Santé F-P-T en septembre 2001. Sa finalité consiste à fournir aux responsables de l’élaboration de politiques et aux gestionnaires des régimes d’assurance-médicaments des analyses critiques sur les tendances relatives aux prix, à l’utilisation et aux coûts des médicaments, afin que le système de soins de santé du Canada dispose de renseignements plus exhaustifs et plus exacts sur la façon dont les médicaments d’ordonnance sont utilisés et sur les sources des augmentations de coût.
Le Comité consultatif du SNIUMP, constitué de représentants des régimes publics d’assurance-médicaments de la Colombie-Britannique, de l’Alberta, de la Saskatchewan, du Manitoba, de l’Ontario, du Nouveau-Brunswick, de la Nouvelle-Écosse, de l’Île du-Prince-Édouard, de Terre-Neuve et-Labrador et du Yukon, et Santé Canada, conseillent le CEPMB à l’égard de son programme de recherche et d’études individuelles. Le Comité comprend également des observateurs de l’Institut canadien d’information sur la santé (ICIS) et de l’Agence canadienne des médicaments et des technologies de la santé (ACMTS).
Le CEPMB a publié cinq rapports du SNIUMP en 2013-2014 :
- L’Observateur des médicaments émergents – 5e édition (décembre 2013)
- Les facteurs de coût associés aux dépenses en médicaments d’ordonnance – Un rapport méthodologique (décembre 2013)
- Analyse éclair : Comparaisons des prix internationaux des médicaments génériques, début 2011 (août 2013)
- L’utilisation de bandelettes de test glycémique dans certains régimes publics d’assurance-médicaments, 2008 (avril 2013)
- L’Observateur des médicaments émergents – 4e édition (avril 2013)
D’autres études du SNIUMP sont en cours d’élaboration et sont résumées dans le programme de recherche du SNIUMPxvii.
Services internes
Description
Les services internes sont des groupes d’activités et de ressources connexes qui sont gérés de façon à répondre aux besoins des programmes et des autres obligations générales d’une organisation. Ces groupes sont les suivants : services de gestion et de surveillance, services des communications, services juridiques, services de gestion des ressources humaines, services de gestion des finances, services de gestion de l’information, services des technologies de l’information, services de gestion des biens, services de gestion du matériel, services de gestion des acquisitions et services de gestion des voyages et autres services administratifs. Les services internes comprennent uniquement les activités et les ressources destinées à l’ensemble d’une organisation et non celles fournies à un programme particulier.
Ressources financières budgétaires (dollars)
| Budget principal des dépenses 2013-2014 |
Dépenses prévues 2013-2014 |
Autorisations totales pouvant être utilisées 2013-2014 |
Dépenses réelles (autorisations utilisées) 2013-2014 |
Écart (dépenses réelles moins dépenses prévues) 2013-2014 |
| 2 833 939 |
3 068 439 |
3 250 531 |
2 998 175 |
(70 264) |
Ressources humaines (ETP)
| Prévu 2013-2014 |
Réel 2013-2014 |
Écart (nombre réel moins nombre prévu) 2013-2014 |
| 19,0 |
22,3 |
*3,3 |
| * Trois ressources ont été temporairement réaffectées des activités de programme pour soutenir la mise en œuvre d’un système de gestion de documents électroniques, pour appuyer les activités de surveillance des RH et pour épauler les activités administratives. |
Analyse du rendement et leçons retenue
En 2013-2014, le CEPMB a publié son Code de conduite, qui est un énoncé des principes fondamentaux et des normes connexes de conduite qui s’appliquent à tous ses employés. En s’engageant à suivre ces valeurs et à adhérer au comportement attendu, le CEPMB renforce la culture éthique du secteur public et contribue à la confiance que fait le public à l’intégrité de toutes les institutions publiques.
En outre, le CEPMB a révisé son instrument de délégation des pouvoirs de signature des documents financiers, qui a reçu l’approbation du ministre. L’objectif principal de cet instrument consiste à documenter les pouvoirs en matière de finances et d’approvisionnement qui sont délégués au CEPMB et de satisfaire aux exigences juridiques du ministre voulant que les délégations soient officiellement effectuées par écrit. Le CEPMB a également réalisé d’importants progrès à l’égard de son système de gestion des documents et des dossiers électroniques (appelé Système de gestion de l’information et des dossiers et des données – SGID). À l’appui de cette initiative, il a également offert à tous ses employés des séances de formation sur le sujet « Devoir de supprimer » et « Soin et garde » des fonds d’information. Par ailleurs, tous les employés du CEPMB sont tenus de suivre le cours en ligne Tenue de documents pour les fonctionnaires proposé par l’École de la fonction publique du Canada.
Section III : Renseignements supplémentaires
Faits saillants des états financiers
Conseil d’examen du prix des médicaments brevetés
État condensé des opérations et de la situation financière nette ministérielle
(non audité)
Pour l’exercice se terminant le 31 mars 2014
(dollars)
| |
Résultats attendus 2013-2014 |
Résultats réels 2013-2014 |
Résultats réels 2012-2013 |
Écart (résultats réels 2013-2014 moins résultats attendus 2013-2014) |
Écart (résultats réels 2013-2014 moins résultats réels 2012-2013) |
| Total des charges |
*12 083 054 |
8 749 006 |
8 338 846 |
(3 334 048) |
410 160 |
| Total des revenus |
**0 |
213 |
0 |
213 |
213 |
| Coût de fonctionnement net avant le financement du gouvernement et les transferts |
12 083 054 |
8 748 793 |
8 338 846 |
(3 334 261) |
409 947 |
| Situation financière nette du ministère |
(925 805) |
(467 168) |
(636 797) |
458 637 |
169 629 |
* Les dépenses prévues en 2013 2014 sont fondées sur l’hypothèse que le CEPMB dépensera la totalité des 2,47 millions de dollars conservés dans l’ABS et réservés pour la tenue d’audiences publiques. La raison en est que ces dépenses dépendent du nombre d’audiences, de la durée et de la complexité des audiences qui se dérouleront, qui sont difficiles à prévoir.
** Les dépenses qui sont non disponibles ne peuvent être utilisées par le Conseil pour s’acquitter de ses obligations. Les revenus non disponibles sont gagnés au nom du gouvernement du Canada. Le CEPMB recueille des revenus non disponibles par suite de paiements effectués par les brevetés au gouvernement du Canada au titre d’Engagements de conformité volontaire ou d’ordonnances du Conseil pour compenser les revenus excédentaires. En 2013 2014, le CEPMB a recueilli des revenus non disponibles d’un montant de 10 605 100 $. En 2012-2013, les revenus non disponibles étaient de 19 670 400 $. |
Conseil d’examen du prix des médicaments brevetés
État condensé de la situation financière (non audité)
Au 31 mars 2014
(dollars)
| |
2013–2014 |
2012–2013 |
Écart (2013-2014 moins 2012-2013) |
| Total des passifs nets |
1 112 115 |
1 228 638 |
(116 523) |
| Total des actifs financiers nets |
571 604 |
525 891 |
45 713 |
| Dette nette du ministère |
540 511 |
702 747 |
(162 236) |
| Total des actifs non financiers |
73 343 |
65 950 |
7 393 |
| Situation financière nette du ministère |
467 168 |
636 797 |
(169 629) |
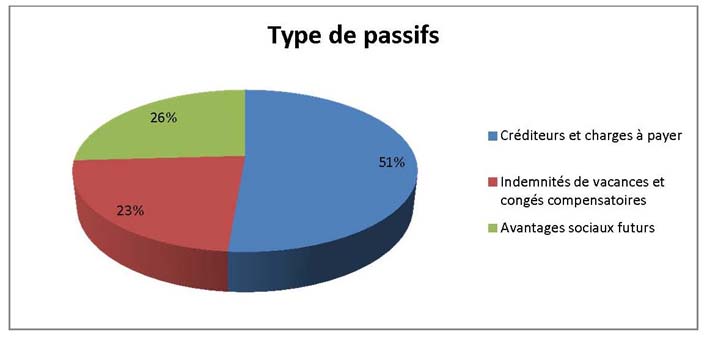
Total des passifs
Le total des passifs nets était de 1 112 115 dollars à la fin de 2013-2014, soit une diminution de 116 523 dollars par rapport à l'exercice précédent. La diminution comportait principalement ce qui suit :
- Une augmentation de 32 444 dollars au titre des créditeurs et charges à payer.
- Une diminution de 7 340 dollars au titre des indemnités de vacances et congés compensatoires.
- Une diminution de 141 627 dollars au titre des avantages sociaux futurs.
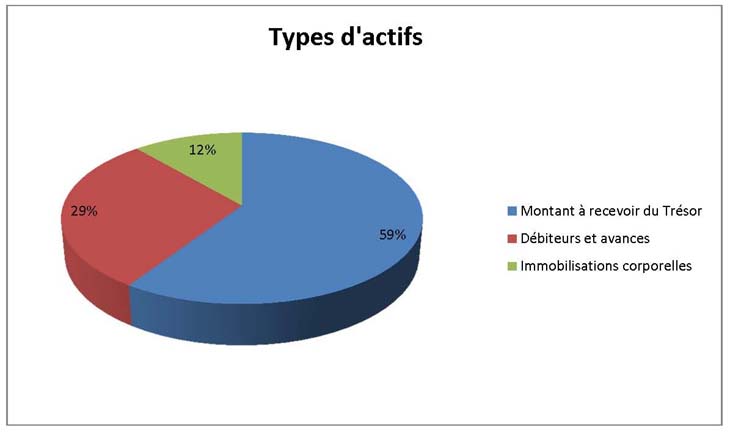
Total des actifs
Total des actifs était 644 947 de dollars à la fin de 2013-2014, une augmentation de 53 106 de dollars par rapport à l'exercice précédent. Les écarts dans les actifs comportaient principalement ce qui suit :
- Une augmentation de 29 214 de dollars au titre du montant à recevoir du Trésor.
- Une augmentation de 16 499 de dollars au titre des débiteurs et avances.
- Une augmentation de 7 393 de dollars au titre des immobilisations corporelles.
États financiers
Les principales données financières présentées dans le présent Rapport ministériel sur le rendement ont pour but de fournir un aperçu général de la position financière et des opérations du CEPMB. Les États financiersxviii du CEPMB sont accessibles sur son site Web.
Tableaux de renseignements supplémentaires
Les tableaux de renseignements supplémentairesxix énumérés dans le Rapport ministériel sur le rendement 2013-2014 se trouvent sur le site Web du Conseil d’examen du prix des médicaments brevetés.
Dépenses fiscales et évaluations
Il est possible de recourir au régime fiscal pour atteindre des objectifs de la politique publique en appliquant des mesures spéciales, comme de faibles taux d’impôt, des exemptions, des déductions, des reports et des crédits. Le ministère des Finances Canada publie annuellement des estimations et des projections du coût de ces mesures dans une publication intitulée Dépenses fiscales et évaluationsxx. Les mesures fiscales présentées dans ladite publication relèvent de la seule responsabilité du ministre des Finances.
Section IV : Coordonnées de l’organisation
Le Conseil d’examen du prix des médicaments brevetés
Case L40
Centre Standard Life
333, avenue Laurier Ouest
Bureau 1400
Ottawa (Ontario) K1P 1C1
Téléphone : 613-952-7360
Sans frais : 1-877-861-2350
Télécopieur : 613-952-7626
ATS : 613-957-4373
Courriel : pmprb@pmprb-cepmb.gc.ca
Site Web : www.pmprb-cepmb.gc.ca
Annexe : Définitions
Architecture d’alignement des programmes : Répertoire structuré de tous les programmes d’un ministère ou organisme qui décrit les liens hiérarchiques entre les programmes et les liens aux résultats stratégiques auxquels ils contribuent.
Cadre pangouvernemental : Schéma représentant la contribution financière des organisations fédérales qui dépendent de crédits parlementaires en harmonisant leurs programmes avec un ensemble de 16 secteurs de résultat pangouvernementaux de haut niveau regroupés sous 4 secteurs de dépenses.
Cible : Niveau mesurable du rendement ou du succès qu’une organisation, un programme ou une initiative prévoit atteindre dans un délai précis. Une cible peut être quantitative ou qualitative.
Crédit : Autorisation donnée par le Parlement d’effectuer des paiements sur le Trésor.
Dépenses budgétaires : Les dépenses budgétaires comprennent les dépenses de fonctionnement et en capital; les paiements de transfert à d’autres ordres de gouvernement, à des organisations ou à des particuliers; et les paiements à des sociétés d’État.
Dépenses non budgétaires : Recettes et décaissements nets au titre de prêts, de placements et d’avances, qui modifient la composition des actifs financiers du gouvernement du Canada.
Dépenses prévues : En ce qui a trait aux RPP et aux RMR, les dépenses prévues s’entendent des montants approuvés par le Conseil du Trésor au plus tard le 1er février. Elles peuvent donc comprendre des montants qui s’ajoutent aux dépenses prévues indiquées dans le budget principal des dépenses.
Un ministère est censé être au courant des autorisations qu’il a demandées et obtenues. La détermination des dépenses prévues relève du ministère, et ce dernier doit être en mesure de justifier les dépenses et les augmentations présentées dans son RPP et son RMR.
Équivalent temps plein : Mesure utilisée pour déterminer dans quelle mesure un employé représente une année-personne complète dans le budget ministériel. L’équivalent temps plein est calculé en fonction du coefficient des heures de travail assignées et des heures normales de travail. Les heures normales de travail sont établies dans les conventions collectives.
Indicateur de rendement : Moyen qualitatif ou quantitatif de mesurer un extrant ou un résultat en vue de déterminer le rendement d’une organisation, d’un programme, d’une politique ou d’une initiative par rapport aux résultats attendus.
Plan : Exposé des choix stratégiques qui montre comment une organisation entend réaliser ses priorités et obtenir les résultats connexes. De façon générale, un plan explique la logique qui sous tend les stratégies retenues et tend à mettre l’accent sur des mesures qui se traduisent par des résultats attendus.
Priorité : Plan ou projet qu’une organisation a choisi de cibler et dont elle rendra compte au cours de la période de planification. Il s’agit de ce qui importe le plus ou qui doit être fait en premier pour appuyer la réalisation du ou des résultats stratégiques souhaités.
Programme : Groupe d’intrants constitué de ressources et d’activités connexes qui est géré pour répondre à des besoins précis et pour obtenir les résultats visés, et qui est traité comme une unité budgétaire.
Programme temporisé : Programme ayant une durée fixe et dont le financement et l’autorisation politique ne sont pas permanents. Ce programme est aussi appelé programme à durée temporaire ou programme à élimination graduelle. Lorsqu’un tel programme arrive à échéance, une décision doit être prise quant à son maintien. Dans le cas d’un renouvellement, la décision précise la portée, le niveau de financement et la durée.
Rapport ministériel sur le rendement : Rapport traitant des réalisations concrètes d’une organisation qui dépend de crédits parlementaires au regard des plans, des priorités et des résultats attendus exposés dans le rapport sur les plans et les priorités correspondant. Ce rapport est déposé au Parlement à l’automne.
Rapport sur les plans et les priorités : Rapport fournissant des renseignements au sujet des plans et du rendement prévu sur trois ans d’une organisation qui dépend de crédits parlementaires. Ces rapports sont déposés au Parlement chaque printemps.
Production de rapports sur le rendement : Processus de communication d’information sur le rendement fondée sur des éléments probants. La production de rapports sur le rendement appuie la prise de décisions, la responsabilisation et la transparence.
Rendement : Utilisation qu’une organisation a faite de ses ressources en vue d’obtenir ses résultats, mesure dans laquelle ces résultats se comparent à ceux que l’organisation souhaitait obtenir, et mesure dans laquelle les leçons apprises ont été cernées.
Résultat : Conséquence externe attribuable en partie aux activités d’une organisation, d’une politique, d’un programme ou d’une initiative. Les résultats ne relèvent pas d’une organisation, d’une politique, d’un programme ou d’une initiative unique, mais ils s’inscrivent dans la sphère d’influence de l’organisation.
Résultat stratégique : Avantage durable et à long terme pour les Canadiens qui est rattaché au mandat, à la vision et aux fonctions de base d’une organisation.
Résultats du gouvernement du Canada : Ensemble de 16 objectifs de haut niveau établis pour l’ensemble du gouvernement et regroupés selon 4 secteurs de dépenses : affaires économiques, affaires sociales, affaires internationales et affaires gouvernementales.
Structure de la gestion, des ressources et des résultats : Cadre exhaustif comprenant l’inventaire des programmes, des ressources, des résultats, des indicateurs de rendement et de l’information de gouvernance d’une organisation. Les programmes et les résultats sont présentés d’après le lien hiérarchique qui les unit, et les résultats stratégiques auxquels ils contribuent. La Structure de la gestion, des ressources et des résultats découle de l’architecture d’alignement des programmes.
Notes de fin de document
i. Des renseignements supplémentaires sur les modifications du Règlement sur les médicaments brevetés sont disponibles sur le site Web du CEPMB à l’adresse : http://www.pmprb-cepmb.gc.ca/view.asp?ccid=786
ii. Loi sur les brevets http://laws-lois.justice.gc.ca/fra/lois/P-4/index.html
iii. Règlement sur les médicaments brevetés http://laws-lois.justice.gc.ca/fra/reglements/DORS-94-688/index.html
iv. Des renseignements supplémentaires sur le Système national d’information sur l’utilisation des médicaments prescrits sont disponibles sur le site Web du CEPMB à l’adresse : http://www.pmprb-cepmb.gc.ca/fr/sniump/à-propos-du-sniump
v. Norme de service pour l’examen scientifique de nouveaux produits médicamenteux brevetés : http://www.pmprb-cepmb.gc.ca/view.asp?ccid=499
vi. Norme de service pour l’examen du prix des nouveaux produits médicamenteux brevetés : http://www.pmprb-cepmb.gc.ca/view.asp?ccid=500
vii. Norme de service pour l’examen du prix des produits médicamenteux brevetés existants : http://www.pmprb-cepmb.gc.ca/view.asp?ccid=501
viii. L’Observateur de médicaments émergents, avril 2013 : http://www.pmprb-cepmb.gc.ca/view.asp?ccid=942
ix. L’utilisation de bandelettes de test glycémique dans certains régimes publics d’assurance-médicaments, 2008, avril 2013 : http://www.pmprb-cepmb.gc.ca/view.asp?ccid=941
x. Analyse éclair – Comparaisons des prix internationaux des médicaments génériques, début 2011, août 2013 : http://www.pmprb-cepmb.gc.ca/view.asp?ccid=487
xi. Les facteurs de coût associés aux dépenses en médicaments d’ordonnance – Un rapport méthodologique, décembre 2013 : http://www.pmprb-cepmb.gc.ca/view.asp?ccid=887
xii. L’Observateur de médicaments émergents, décembre 2013 : http://www.pmprb-cepmb.gc.ca/view.asp?ccid=483
xiii. Plan de surveillance et d´évaluation des principales modifications aux Lignes directrices 2013 : http://www.pmprb-cepmb.gc.ca/view.asp?ccid=493
xiv. Des renseignements supplémentaires sur les changements de la Méthodologie de rajustement du prix selon l’IPC et les consultations à ce sujet sont disponibles sur le site Web du CEPMB à l’adresse : http://www.pmprb-cepmb.gc.ca/view.asp?ccid=783
xv. Cadre pangouvernemental, http://www.tbs-sct.gc.ca/ppg-cpr/frame-cadre-fra.aspx
xvi. Comptes publics du Canada 2014, http://www.tpsgc-pwgsc.gc.ca/recgen/cpc-pac/index-fra.html
xvii. Le programme de recherche du SNIUMP est disponible sur le site Web du CEPMB à l’adresse : http://www.pmprb-cepmb.gc.ca/fr/sniump/programme-de-recherche
xviii. Les États financiers du CEPMB sont accessibles sur son site Web : http://www.pmprb-cepmb.gc.ca/fr/view.asp?ccid=1111
xix. Les tableaux de renseignements supplémentaires énumérés dans le Rapport ministériel sur le rendement 2013 2014 se trouvent sur le site Web du Conseil d’examen du prix des médicaments brevetés : http://www.pmprb-cepmb.gc.ca/view.asp?ccid=890
xx. Dépenses fiscales et évaluations, http://www.fin.gc.ca/purl/taxexp-fra.asp